Giving Calcification Its Due: Recognition of a Diverse Disease: A First Attempt to Standardize the Field
Article type: Review
Files: CIRCRESAHA.116.310060.pdf
Publication Year: 2017
Rating: ⭐⭐⭐⭐
Status: Finished
Tags: 其他
重点概括
心血管钙化的机制主要是两大类形式:
- 高磷酸盐的细胞内环境:SMC/VIC 摄取磷酸盐,与胞内调节因子结合,细胞释放不含TNAP的细胞外囊泡(EVs)。形成的矿物沉积中的磷元素来自内环境中的磷酸盐。这种钙化可以称为不依赖碱性磷酸酶的钙化,需要内环境中具有高磷酸盐。
- 脂质沉积炎症条件下:巨噬细胞等炎症细胞参与下,SMC/VIC 向成骨细胞分化,成骨细胞分泌的囊泡中含有TNAP,其可以将细胞内的磷酸源(有机物中的磷酸,如ATP)转化为游离的无机磷酸盐。这种钙化可以称为依赖碱性磷酸酶的钙化,SMC/VIC 的成骨分化是其发生的始动环节。
![图片[1]-Giving Calcification Its Due: Recognition of a Diverse Disease: A First Attempt to Standardize the Field-香草杏仁](https://rotterltblog.oss-cn-shanghai.aliyuncs.com/posts/Untitled-20220501152212-m6up7er.png)
疑问
原文梳理
血管钙化VS瓣膜钙化
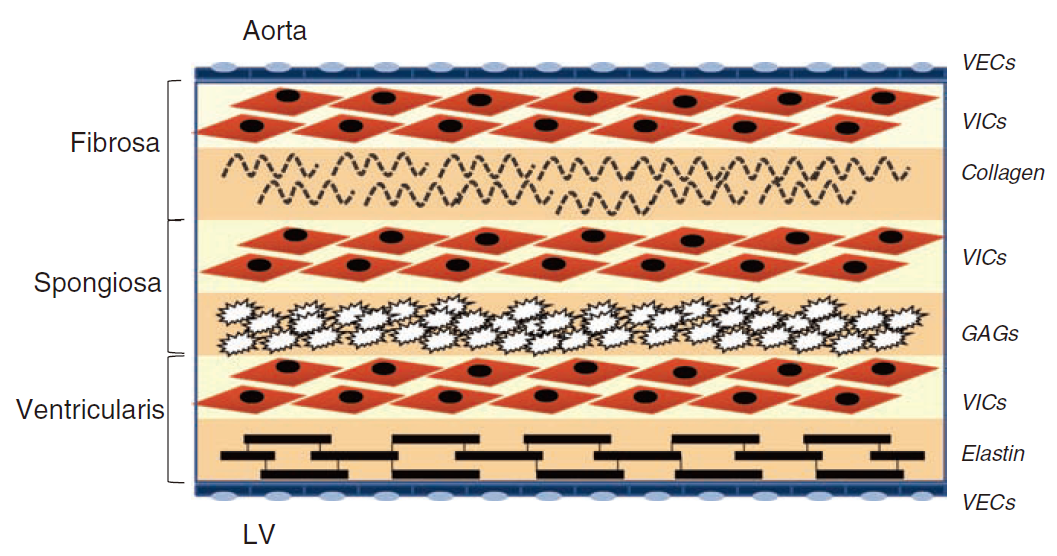
组织结构的区别:血管是由富含胶原以及富含弹力蛋白的两层结构组成,而主动脉瓣是三层结构,胶原纤维、蛋白聚糖、弹力蛋白。
钙化的发生主要有两种形式:一种是高磷酸盐引起的矿物质沉积,另一种是炎症诱发的中膜钙化。这两种钙化形式经常同时出现,但是在机制上是独立的。只有10%~13%的钙化表现为成熟的成骨活动,其余都表现为营养不良性成骨。
常用的三种钙化动物模型:
- 高脂血症(Ldlr−/−, Apoe−/−)
- 高磷酸盐血症(Klotho−/, vitamin D overload)
- 肾功能不全(5/6 nephrectomy))
其他:可用联合模型(Apoe−/−+5/6 nephrectomy)或者直接对主动脉瓣造成网状损伤可以更快诱导钙化。
不同的钙化始动因素
高磷酸盐血症(慢性肾病,中膜钙化)
高磷酸盐血症的体外模型是直接在细胞外进行磷酸盐刺激,SMC和巨噬细胞在刺激下很快发生钙化。细胞外的磷酸盐引起一系列的细胞应答,但是成骨分化和 TNAP(组织非特异性碱性磷酸酶)的高表达不是始动因素。
研究表明,细胞外的磷酸盐会使得矿物质在 SMC 和巨噬细胞分泌的细胞外囊泡中沉积。这些细胞外囊泡的功能与骨基质小泡相似,但两者来自不同的细胞过程且拥有不同的蛋白组学特征。
这种高磷酸盐诱导钙化的体外模型反映的是高磷酸盐血症的体内模型,通过降低肾功能或者增加磷酸盐摄入的方法干扰体内磷酸盐代谢,从而诱发钙化。
高磷酸盐血症的患者发生钙化的速度也很快,钙化是高磷酸盐血症的明确并发症之一。
炎症诱发的钙化
心血管钙化最普遍的形式是在以脂质沉积为特征的炎性斑块中发生,因此,常用高脂血症动物模型来研究这种钙化。这种钙化的发生依赖于TNAP的高表达,其可以将磷酸源转化为无机磷酸盐。
细胞的分化和磷酸盐的生成是限速步骤,于是这种炎症诱发的钙化发生速度相对较慢。
Calcification serves as an end point to inflammation-driven remodeling.
炎症诱发钙化反应的过程中,一旦钙化发生,就与炎症驱动无关了。
研究表明,由于他汀类药物的抗炎作用,如果在钙化开始之前给予他汀治疗可能可以预防钙化,但是一旦已经开始重塑(钙化),他汀可能会加速钙化的发生,甚至直接刺激成骨反应。
在斑块内发生的钙化一开始是由钙化性 EVs 聚合形成的圆形或椭圆形微钙化,这些微钙化进一步融合形成更大的微钙化(相对稳定的斑块),影响瓣膜的正常功能。



暂无评论内容