Chen J, Ren T, Xie L, Hu H, Li X, Maitusong M, Zhou X, Hu W, Xu D, Qian Y, Cheng S, Yu K, Wang JA, Liu X. Enhancing aortic valve drug delivery with PAR2-targeting magnetic nano-cargoes for calcification alleviation. Nat Commun. 2024;15:557.
引言
主动脉瓣钙化病(CAVD)的临床重要性及当前治疗局限性
略
靶向药物递送系统(TDDSs)在治疗 CAVD 中的潜在价值
- 疗效 vs 副作用:常规系统性药物的功效可能受到肝脏代谢、肾脏排泄以及非特异性分布的限制,导致只有相对较小数量的药物到达靶位点。
- 已有研究 TDDS 在腹主动脉瘤中的潜在应用 Lin, W. et al. A multi-bioactive nanomicelle-based “one stone for multiple birds” strategy for precision therapy of abdominal aortic aneurysms. Adv. Mater. 34, e2204455 (2022). 本研究也是基于纳米材料
- 另一种 TDDS:仿生脂质体具有出色的生物相容性和归巢能力,也被尝试应用于心肌梗死和动脉粥样硬化的靶向治疗。Gao, J. F. et al. Precisely co-delivery of protein and ROS scavenger with platesomes for enhanced endothelial barrier preservation against myocardial ischemia reperfusion injury. Chem.Eng.J.446, 136960 (2022).;Song,Y.N.etal.Biomimeticliposomeshybridwithplateletmembranes for targeted therapy of atherosclerosis. Chem.Eng.J.408, https://doi.org/10.1016/j.cej.2020.127296 (2021).
结果
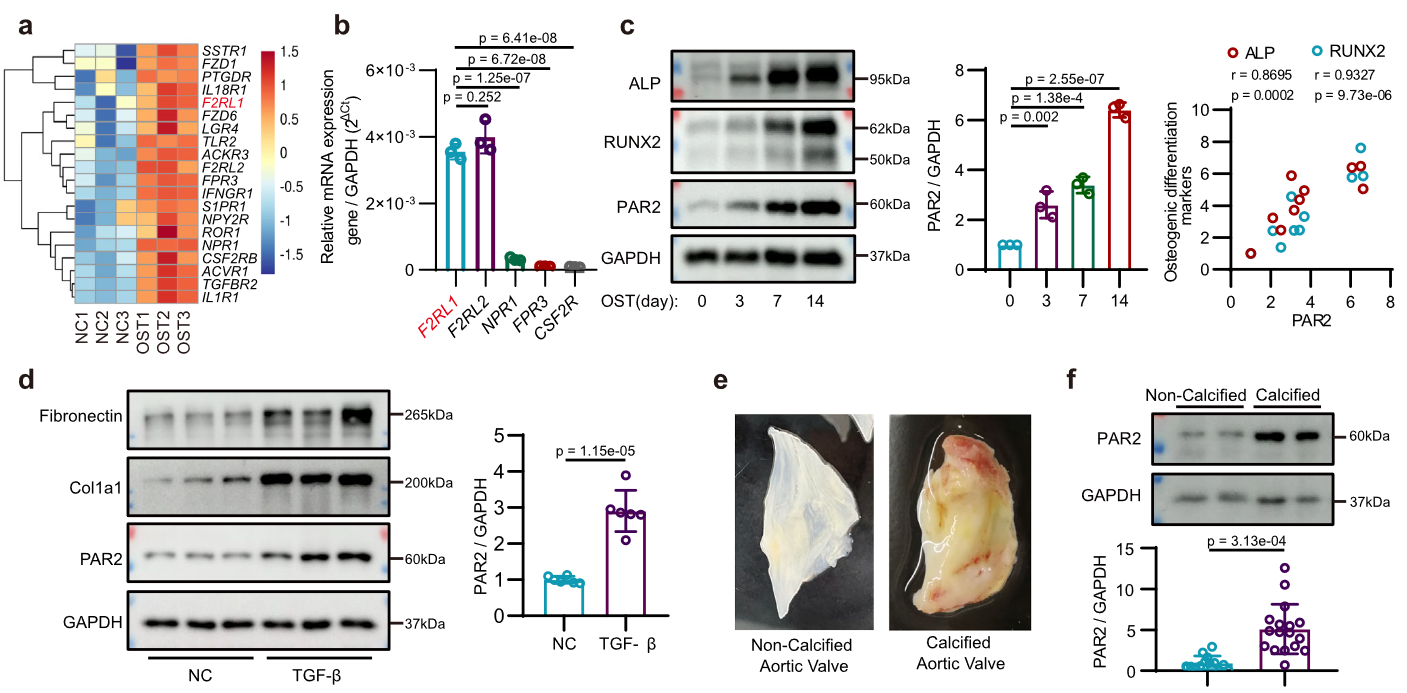
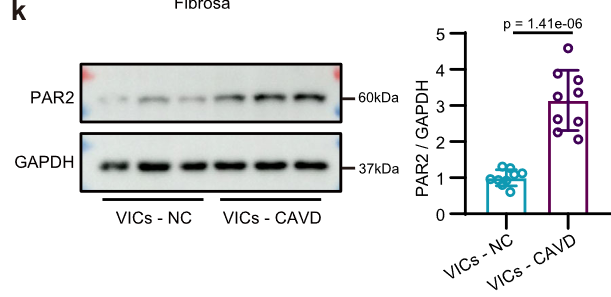
PAR2 在成骨分化的 hVICs 和钙化主动脉瓣中表达增加
-
细胞 RNAseq 和组织蛋白水平分析

-
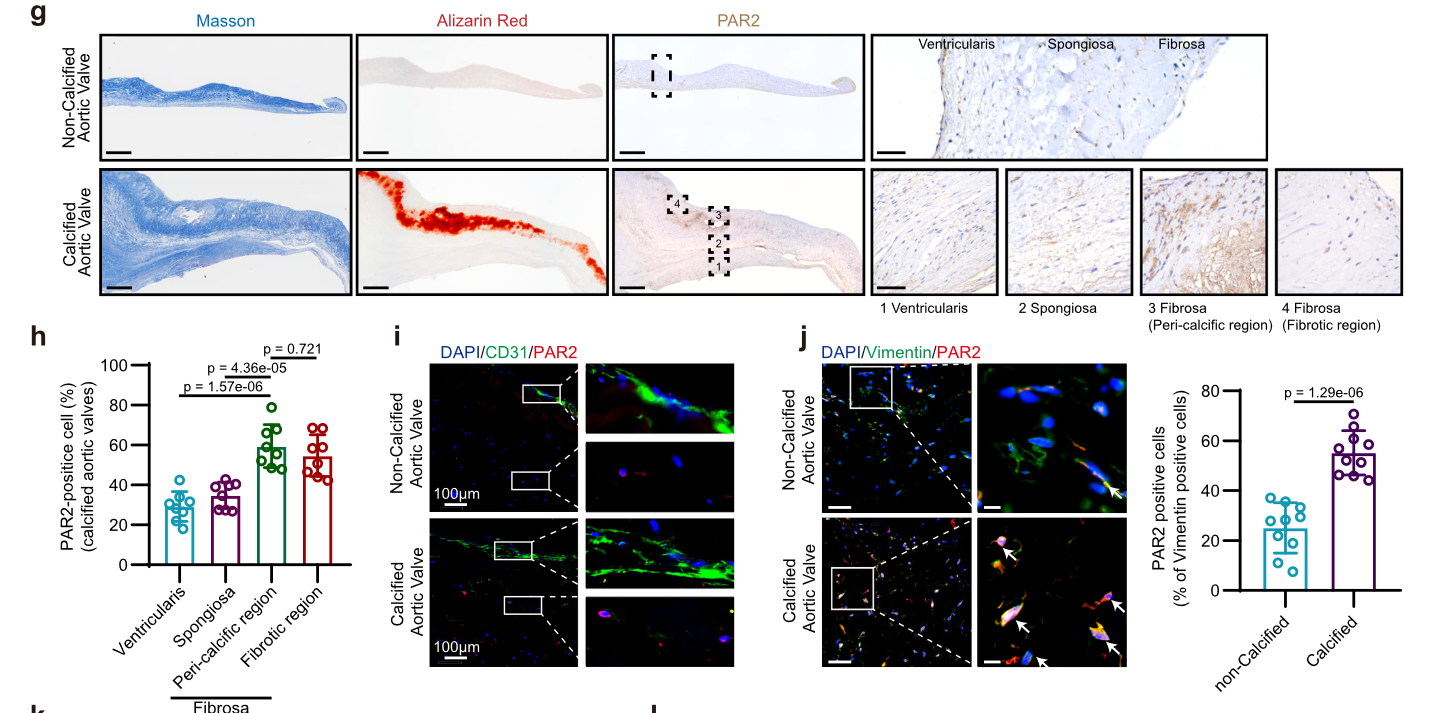
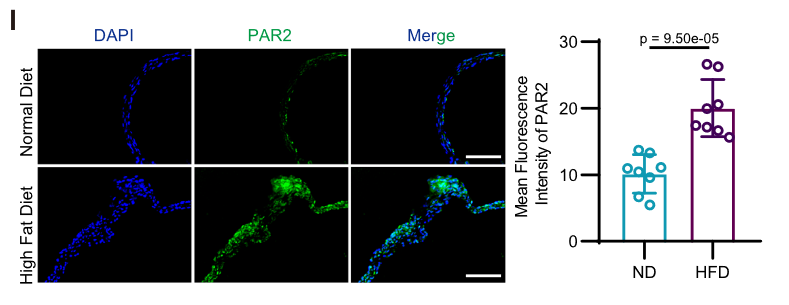
PAR2 的组织学定位

-
组织中分离的 VIC

-
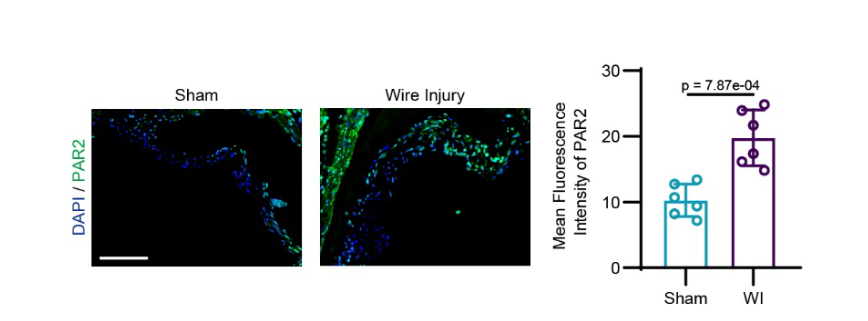
小鼠模型中的验证 (高脂喂养 Ldlr-/-与 8w 导丝损伤双模型)


PAR2 阳性细胞促进瓣膜钙化
cavd 单细胞的分析:
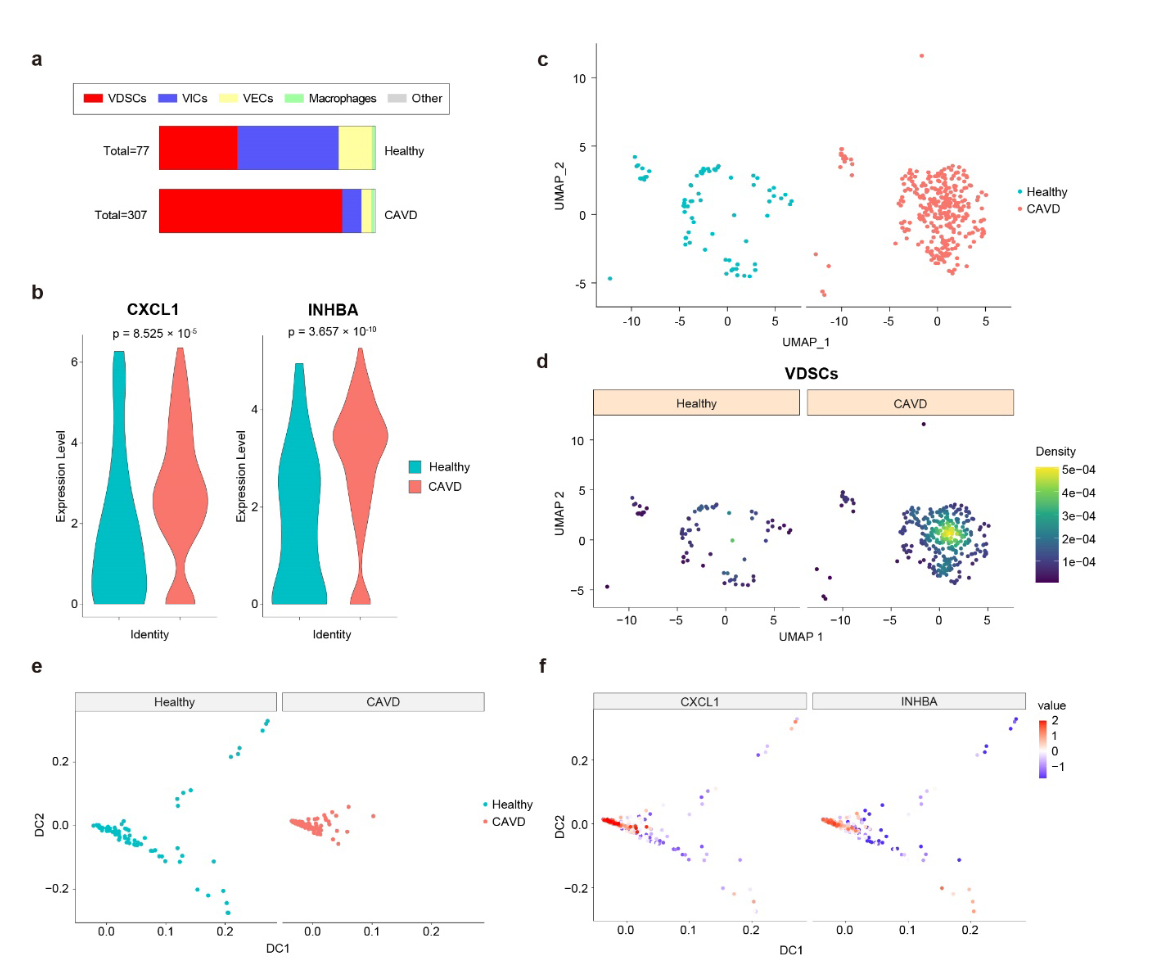
- F2RL1 阳性细胞主要是 VICs 和 VDSCs,而不是 VECs 或巨噬细胞。
- 钙化瓣膜来源的 F2RL1 阳性细胞表现出更高的 INHBA(抑制素 β-A,TGF-β 超家族的成员)表达,代表 TGF-β 通路的激活,以及更高的 CXCL1(编码生长调节的 α 蛋白)表达,表明其具有更强的招募炎性细胞的能力。
- GSEA 显示,表达 VDSCs 相关基因较高的 F2RL1 阳性细胞主要来源于 CAVD
- CXCL1 和 INHBA 的表达沿着 F2RL1 阳性细胞谱系轨迹逐渐增加,表明针对 F2RL1 阳性细胞的靶向干预可能会抑制这一细胞群的发展,从而阻止 CAVD 的进展。
PAR2 配体功能化增强了纳米颗粒与成骨分化的人类瓣膜间充质细胞的结合
-
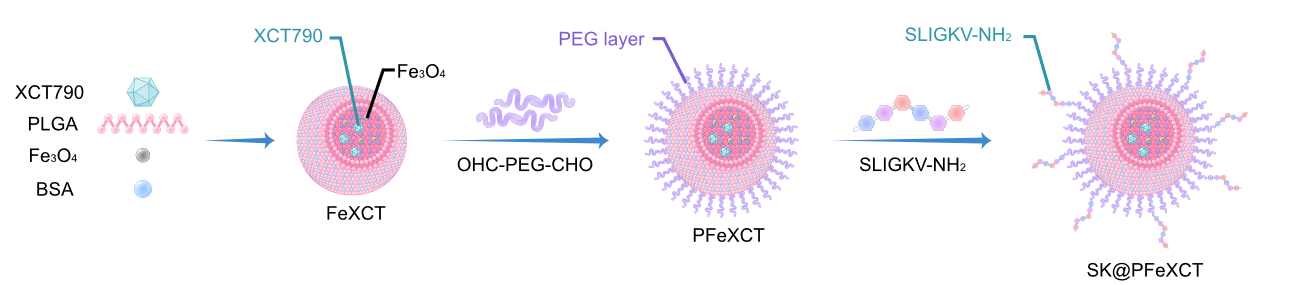
纳米材料的结构图示

- PLGA 是一种具有表面改性潜力的有前途的生物可降解和生物相容性高分子,能够很好地载荷疏水性药物和纳米粒子。作者采用了油包水(O/W)乳液溶剂蒸发法来合成纳米粒子核心,该核心包括 PLGA、XCT790 和 10 纳米的磁性纳米颗粒(MNPs),同时使用溶解在水中的牛血清白蛋白(BSA,一种两亲分子)作为稳定剂
颗粒表面的 BSA 分子提供了氨基,这些氨基通过醛基和氨基的缩合作用与 OHC–PEG–CHO 形成了共价结合。OHC–PEG–CHO 同样作为 PAR2 靶向肽(SLIGKV-NH2 或 SLIGRL-NH2)的交联剂
多肽 SLIGKV-NH2(人)或 SLIGRL-NH2(小鼠)是 PAR2 受体激动剂
- PLGA 是一种具有表面改性潜力的有前途的生物可降解和生物相容性高分子,能够很好地载荷疏水性药物和纳米粒子。作者采用了油包水(O/W)乳液溶剂蒸发法来合成纳米粒子核心,该核心包括 PLGA、XCT790 和 10 纳米的磁性纳米颗粒(MNPs),同时使用溶解在水中的牛血清白蛋白(BSA,一种两亲分子)作为稳定剂
-
颗粒的物理性质鉴定
-

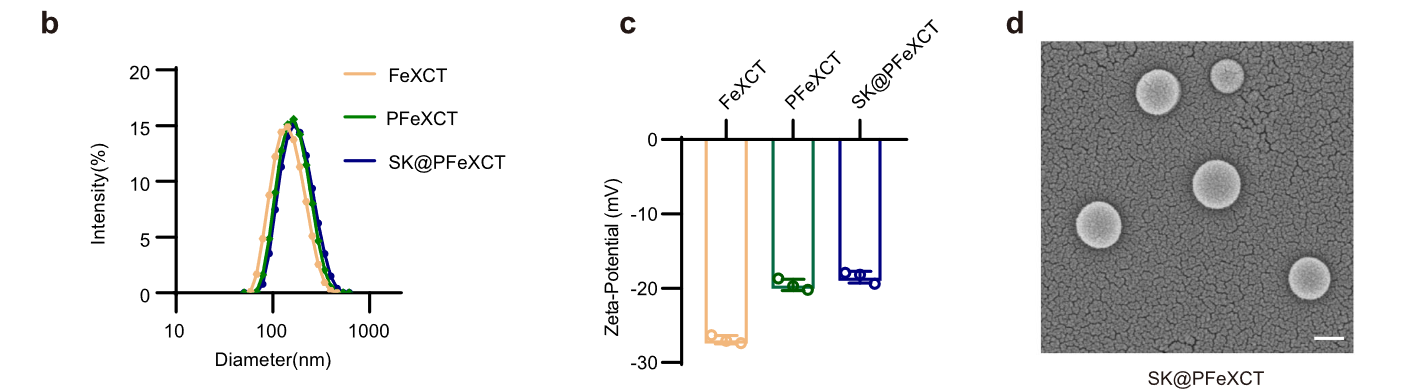
- PLGA 纳米颗粒平均尺寸为 147.4 ± 6.3 nm,修饰后增加到 186.8 ± 6.9 nm,但不影响尺寸分布。
- zeta 电位从-26.93 ± 0.57 mV 增加到-18.50 ± 0.79 mV,这可能是由于带负电的 BSA 被更多中性的 PEG 覆盖。
- 扫描电子显微镜(SEM)证实了 SLIGKV 修饰的、MNPs 和 XCT790 负载的纳米颗粒(SK@PFeXCT)的球形结构;SK@PFeXCT 为 159.4 ± 6.7 nm。
-
-
SK@PFeXCT(笔记中后续简称 SK 粒子)对成骨 VIC 的靶向能力鉴定
- 后续出现的多种粒子或分子简述:
- SK@PFe(功能化的磁性纳米颗粒,但不含有效药物)
- XCT790(单纯的有效药物,未使用磁性纳米颗粒包裹)
- PFeXCT(单纯磁性纳米颗粒包裹 XCT790)
- SK 粒子(即 SK@PFeXCT,SLIGKV-NH2)用于人 VIC 的实验
- SR 粒子(SK@PFeXCT,SLIGRL-NH2)用于小鼠的实验
-

- 后续出现的多种粒子或分子简述:
磁场引导的纳米粒子在人 VICs 中的定位
-
SK 粒子的磁响应属性鉴定
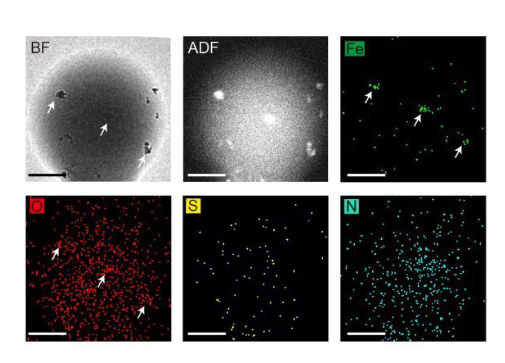
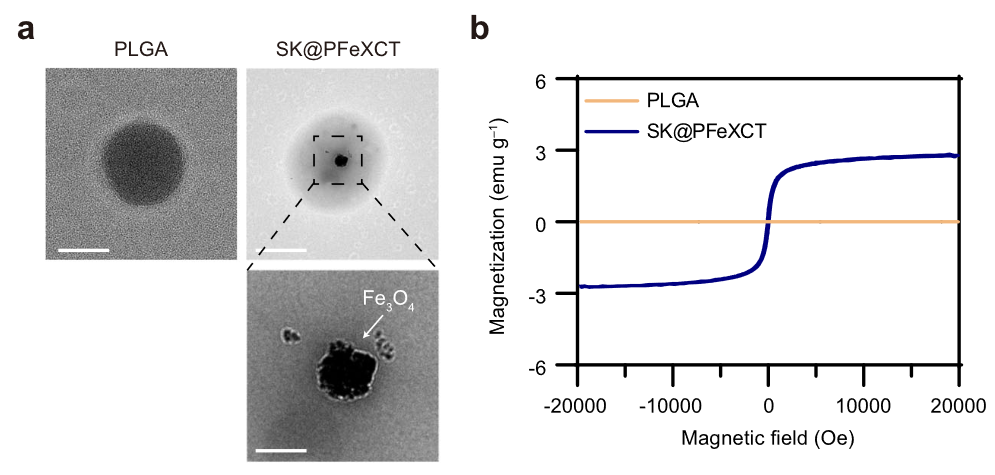
- 在透射电子显微镜(TEM)图像中(图 4a),与裸露的 PLGA 相比,SK 纳米颗粒中可见明显的深色区域。这些深色区域归因于 MNP 的存在,通过环形暗场扫描透射电镜(ADF-STEM)和元素映射(补充图 10)得到证实。通过磁滞回线特性验证了磁响应属性(图 4b)。
-

-

-
SK 粒子与 VIC 的相互作用
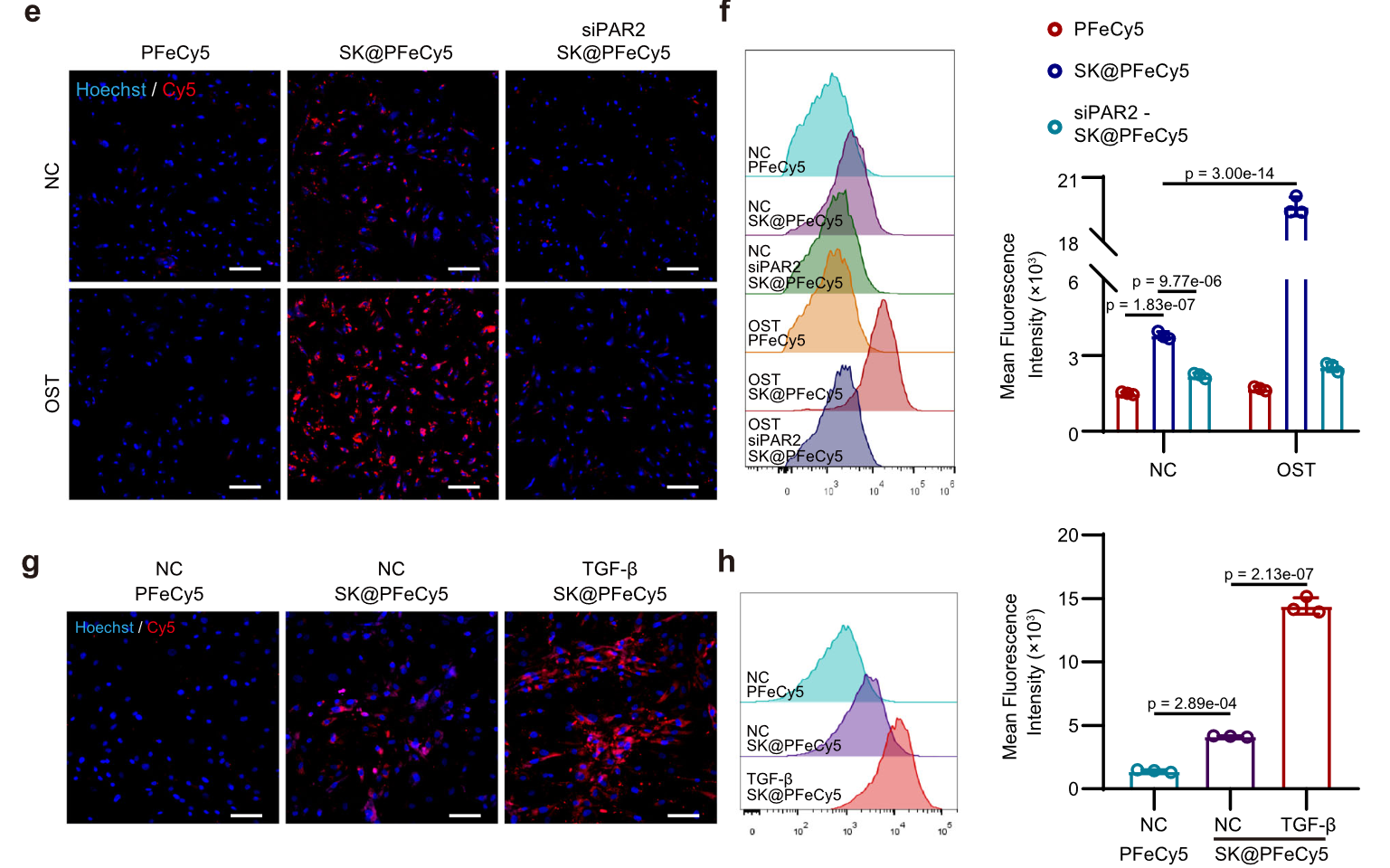
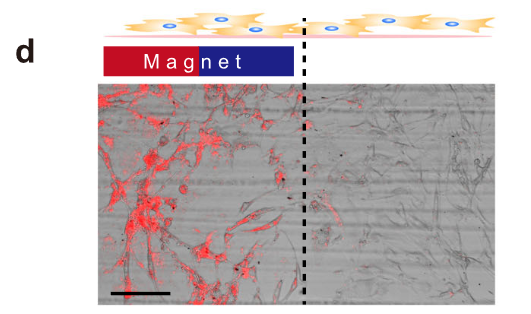
- 静态培养体系的靶向能力验证
-

-

-
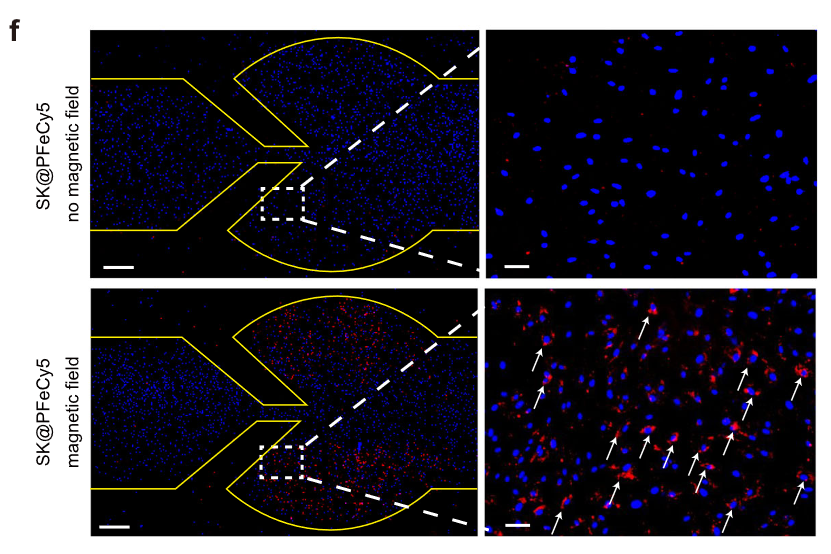
- 动态培养体系(流体培养基)
-

-

-
纳米治疗显著降低 hVIC 成骨分化
-
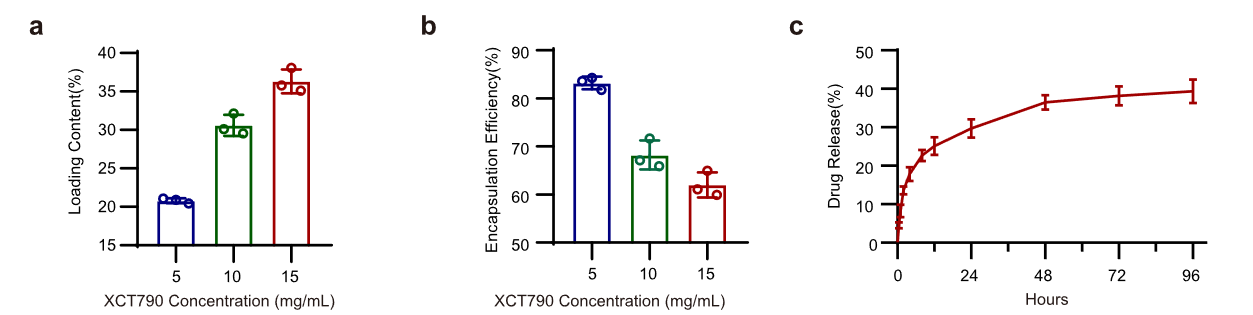
SK 粒子药物荷载量与药物释放曲线
-

- 随着 XCT790 的含量从 5 毫克/毫升(XCT790 在有机相中的浓度)增加到 15 毫克/毫升,纳米颗粒中 XCT790 的加载含量显著增加,从 20.80 ± 0.3274% 增加到 36.33 ± 1.544%,而包封效率则从 82.31 ± 1.313% 下降到 62.00 ± 2.634%(图 5a, b)。因此,选择了 15 毫克/毫升的 XCT790 浓度用于后续实验。 20.80 * 82.31= 1712.048 36.33 * 62=2252.46
-
-
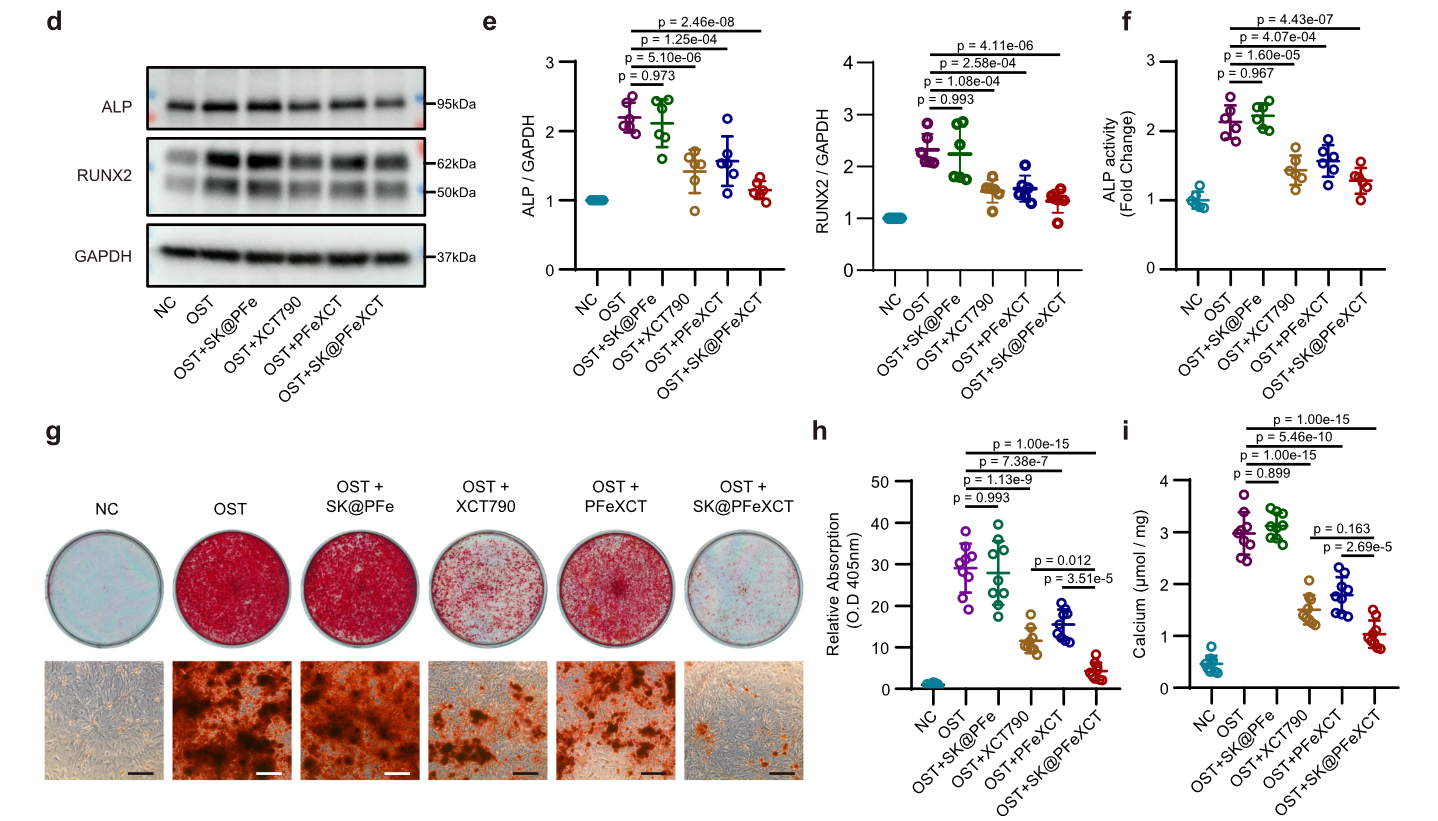
SK 粒子降低成骨培养 VIC 中钙化标记物的表达
-

- 培养时在培养皿底部加了磁场
- 各组降低钙化的能力比较:SK 粒子 > XCT790 > PFeXCT > SK@PFe
- SK 粒子展示了在钙沉积上最强的抑制效果(图 5g, h),可能是因为结合到 PAR2 后粒子被细胞内吞以及 XCT790 的持续细胞内释放,导致更高的细胞内 XCT790 浓度。
- 注:细胞水平的研究同时也使用了小鼠 MOVAS-1 细胞系,结论相同
-
-
纳米疗法(SR 粒子)缓解小鼠主动脉瓣钙化
-
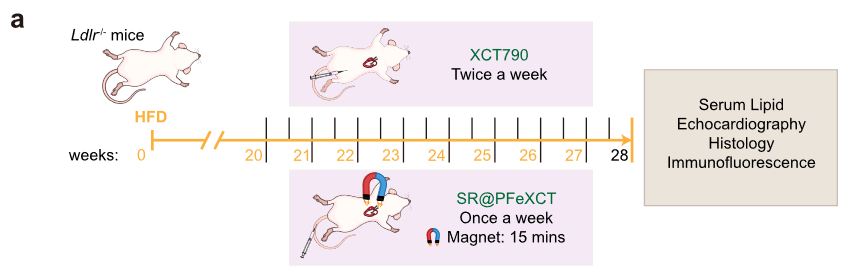
小鼠模型的建立与纳米疗法干预
-

- Ldlr 小鼠先喂养 HFD20w,分组静脉注射 SR@PFe、SR 粒子以及单纯的 XCT790
- 粒子组每周注射 1 次,而 XCT790 组每周给药 2 次
- 共喂养 28w 后检测
-
-
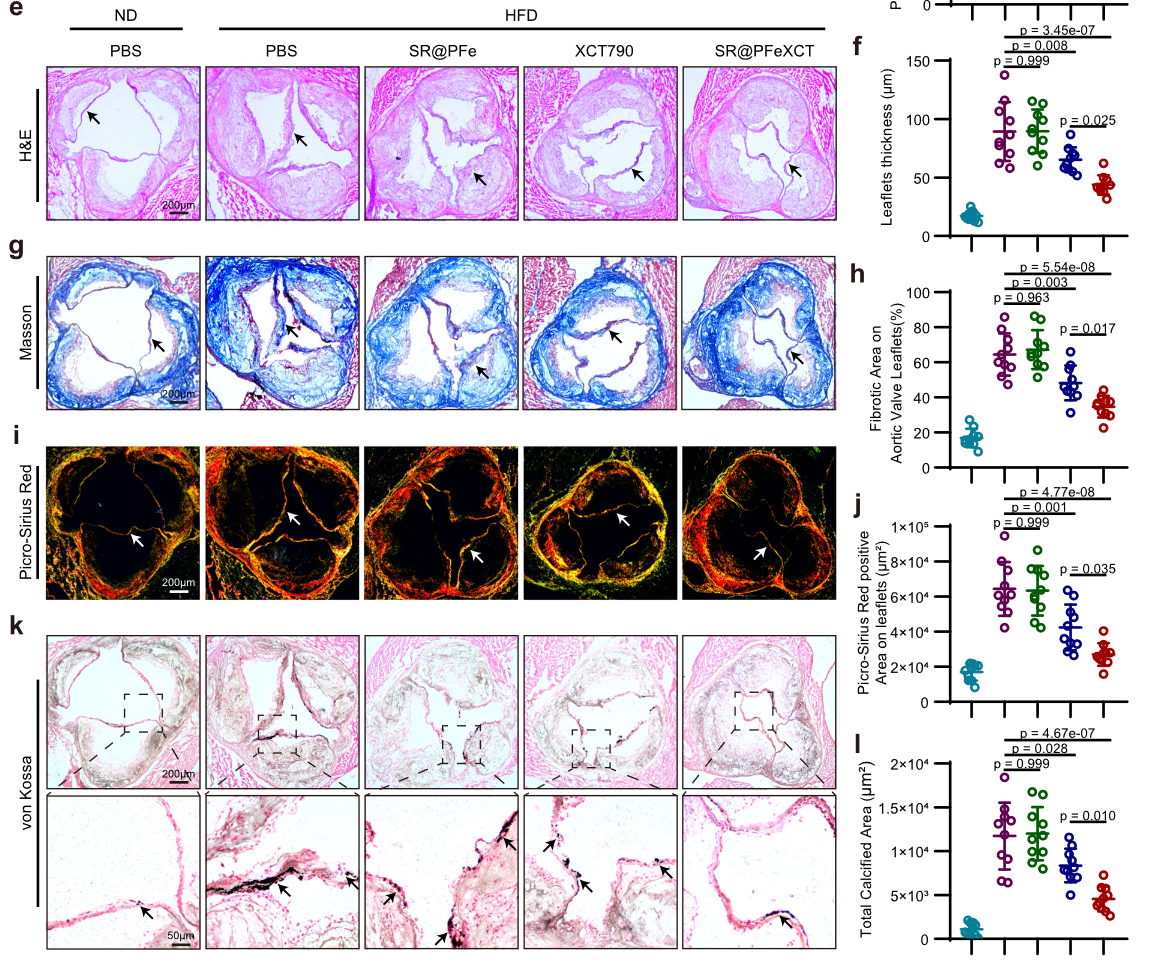
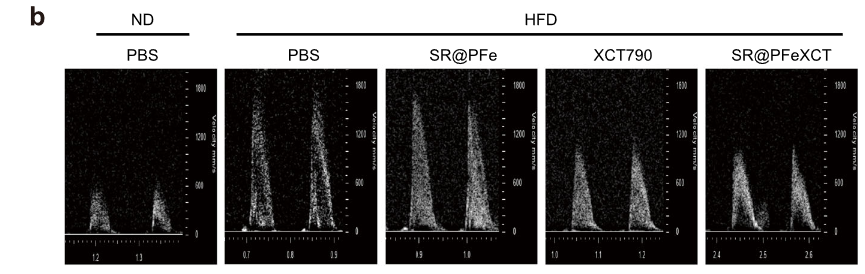
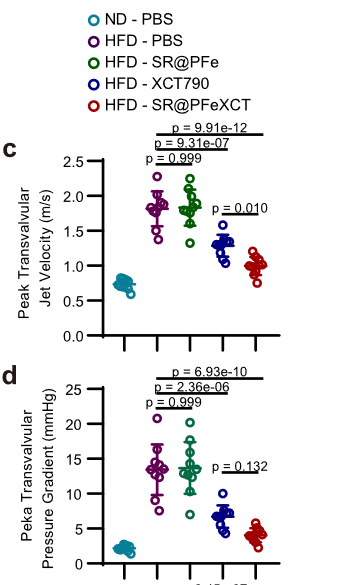
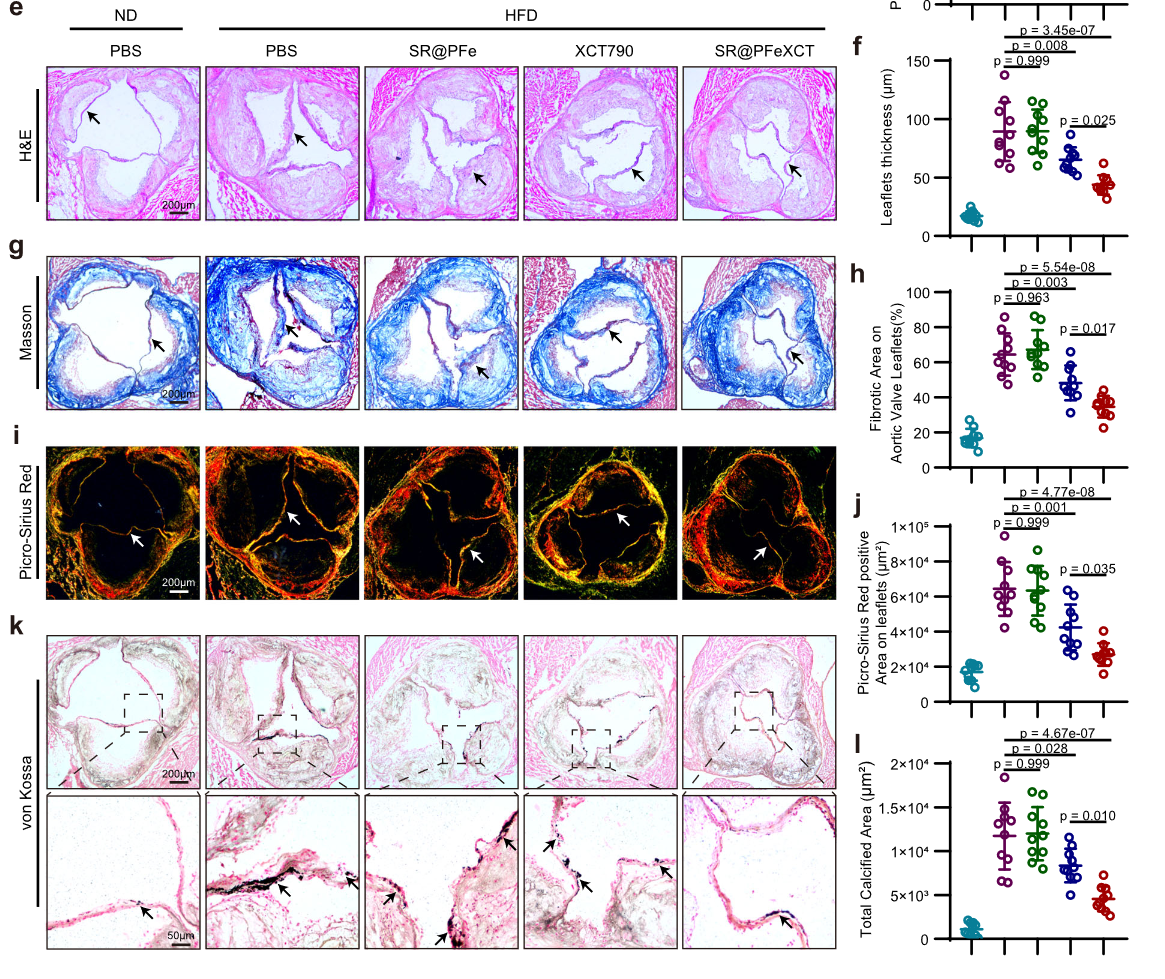
各组疗效比较
-

-

-
-

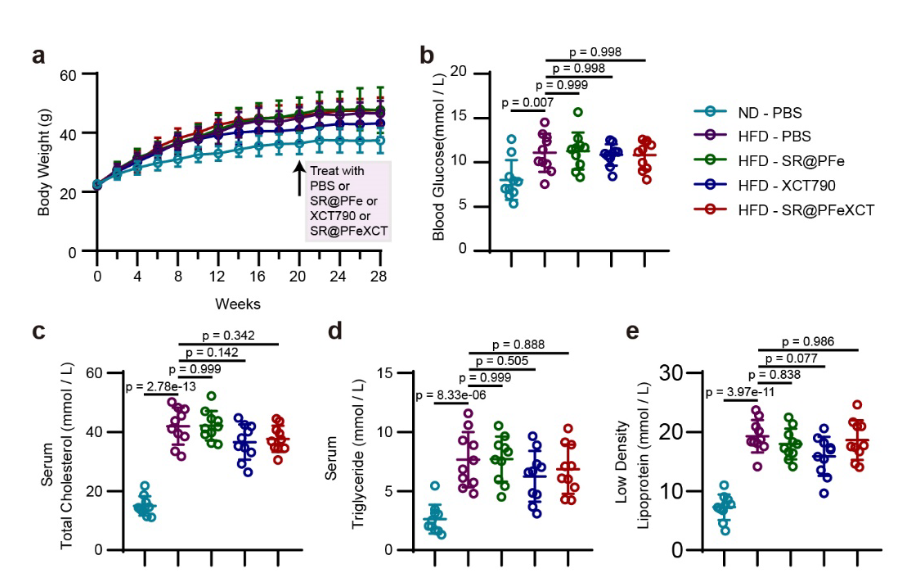
- 为了排除全身代谢因素对瓣膜增厚和钙化的影响,记录了小鼠的体重,并测量了包括血糖、总甘油三酯、总胆固醇和低密度脂蛋白(LDL)在内的代谢参数
-

-
-
代谢重编程介导了纳米治疗的抗钙化效应
- 血管钙化时糖酵解作用增强,代谢中间体可能参与成骨型表型重编程。
- 本研究中选用的药物 XCT790 是 ERRα 的特异性抑制剂,广泛认为是线粒体生物发生和糖酵解的强效调节剂。
-
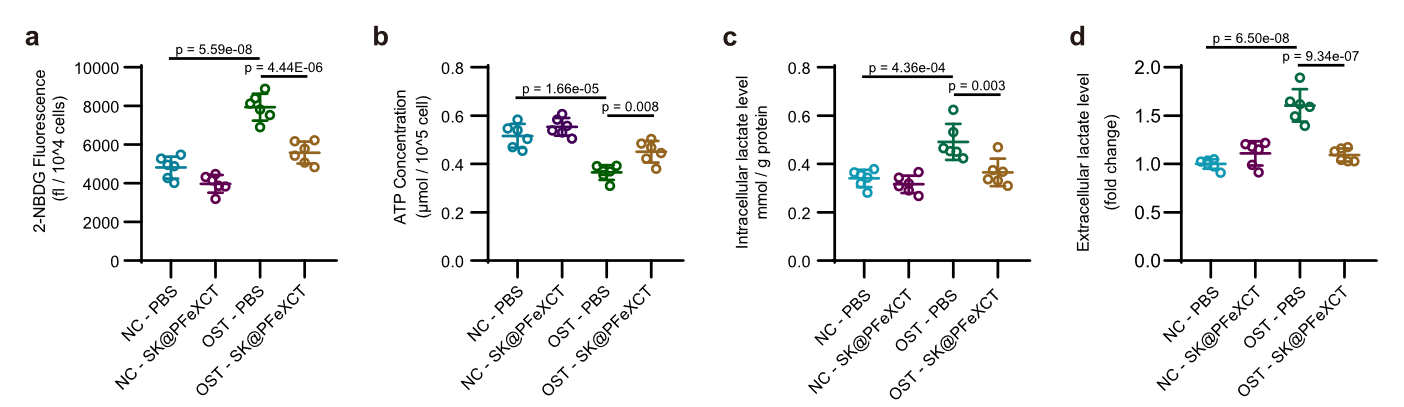
糖的摄取与 ATP 生成差异
- 成骨分化的人类瓣膜间充质细胞比正常的人类瓣膜间充质细胞摄取更多的葡萄糖并产生更少的 ATP;SK 粒子消除了这一变化
- 中间产物乳酸的积累
-

-
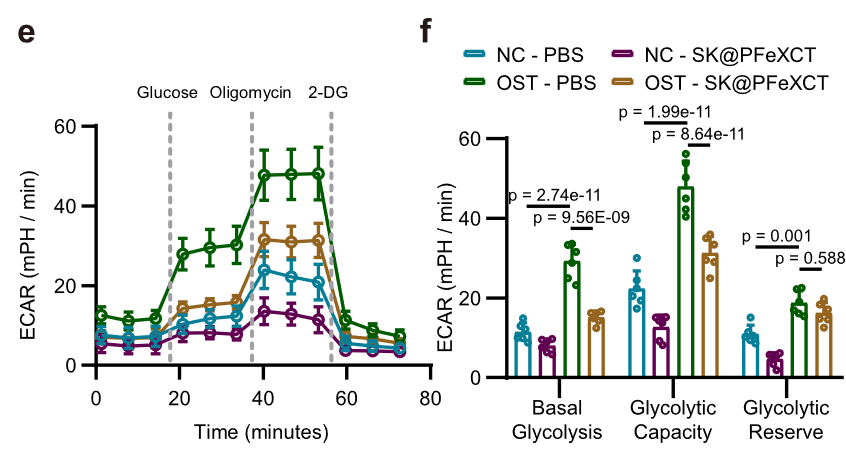
ECAR 检测
- 细胞外酸化率(ECAR)测定进一步确认,在成骨分化过程中,基础糖酵解和总体糖酵解能力得到了增强,而 SK 粒子抑制了这一代谢重编程
-

-
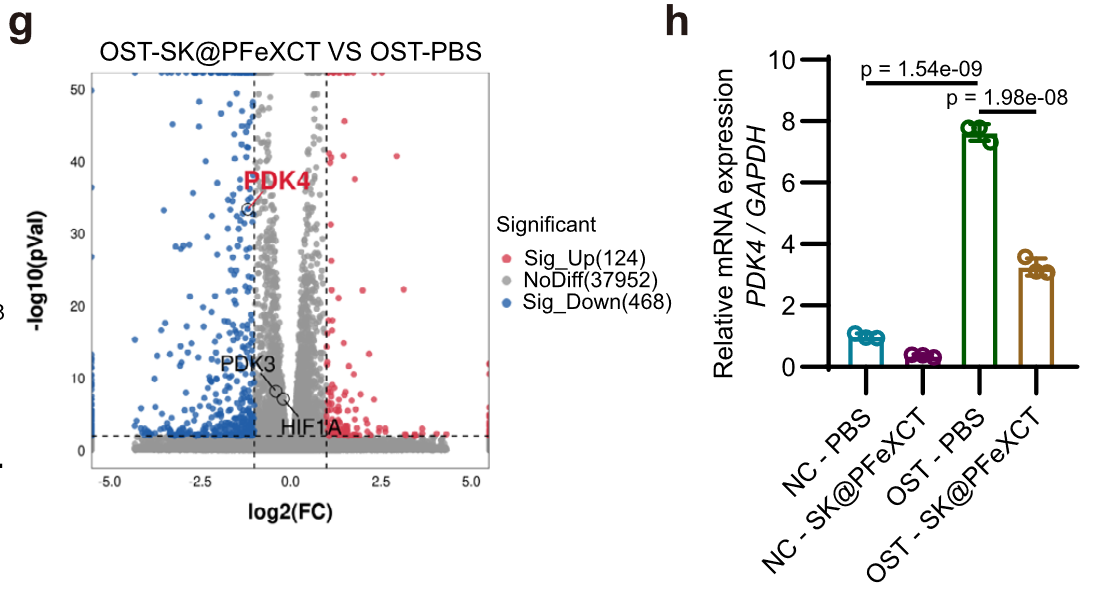
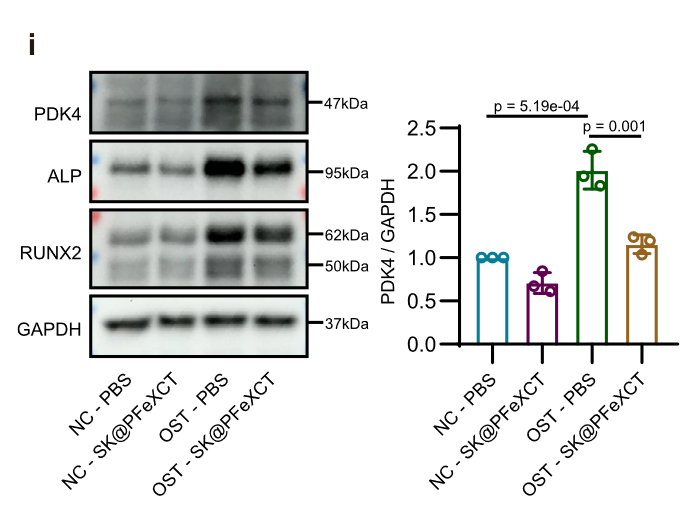
RNA-seq 分析糖酵解相关基因
- PDK4:丙酮酸脱氢酶激酶 4
-

-

-
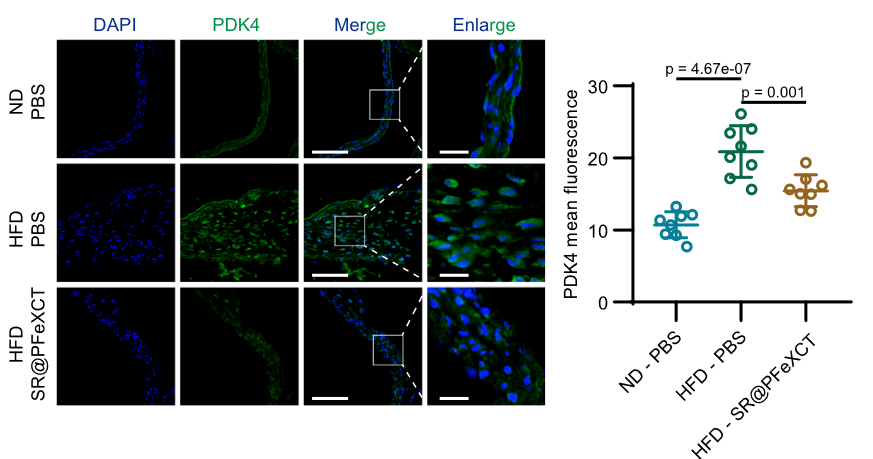
小鼠模型中验证 SR 粒子显著降低 PDK4 水平
-

-
思路回顾
CAVD 中 TDDS 的应用有三大局限:
- 狭窄后主动脉瓣附近的血流速度可超过 4m/s,这阻碍了药物或纳米颗粒在瓣膜内的积累。
- 主动脉瓣不含有毛细血管丛,限制了纳米药物在瓣膜内的进入和滞留
- 缺乏 CAVD 的特异性靶向标记物,这妨碍了主动靶向有效输送药物
如何解决上述局限性?
- 磁导航策略 Magnetic targeting
- 由于对外源性磁场(EMF)的响应性,这种磁场是非侵入性的且能穿透组织,基于磁性纳米粒子(MNPs)的药物传递系统备受期待,特别是用于靶向深层组织。
- 在肿瘤、深部组织感染、缺血性心脑血管疾病中均有相关研究报道
- 虽然在 EMF 引导下,MNPs 能够在病变组织周围富集,但必须增强其药物锚定能力以抵抗狭窄主动脉瓣膜的剧烈血流。此外,为了使纳米颗粒能够作用于引起疾病的 VICs,必须提高靶向精确性。
- 特异性高表达的细胞膜表面标记物能够解决靶向精确性的问题
- 蛋白酶激活受体 2(PAR2)已被暗示与动脉粥样硬化有关
- PAR2 是一个潜在的靶点:结合配体后,PAR2 会被内吞并转移到溶酶体,药物通过靶向 PAR2 递送就能精准进入细胞内。
- 因此,如果在 CAVD 中 PAR2 的蛋白表达上调,它可能用于 CAVD 的靶向药物递送系统。
- 构建 TDDS 不仅要靶向,还需要有效药物
- XCT790 是一种特异性的雌激素相关受体 α(ERRα)拮抗剂,最近发现它能抑制人 VICs 的成骨分化。Hu, W. et al. Knockdown of estrogen-related receptor alpha inhibits valve interstitial cell calcification in vitro by regulating heme oxygenase 1. FASEB J. 35, e21183 (2021). 但其机制尚未阐明
- 在之前的一项研究中筛选的 1595 种药物中,XCT790 在纠正 iPSC 衍生的 VECs 的成骨分化相关转录组紊乱方面最为有效。Theodoris, C. V. et al. Network-basedscreeniniPSC-derivedcells reveals therapeutic candidate for heart valve disease. Science 371, https://doi.org/10.1126/science.abd0724 (2021).
- XCT790 的应用局限性:1. 导致 NASH;2. 其受体在核内。
文章的整体思路实际上就是在解决以上局限性(科学问题),顺便做了后续的机制验证
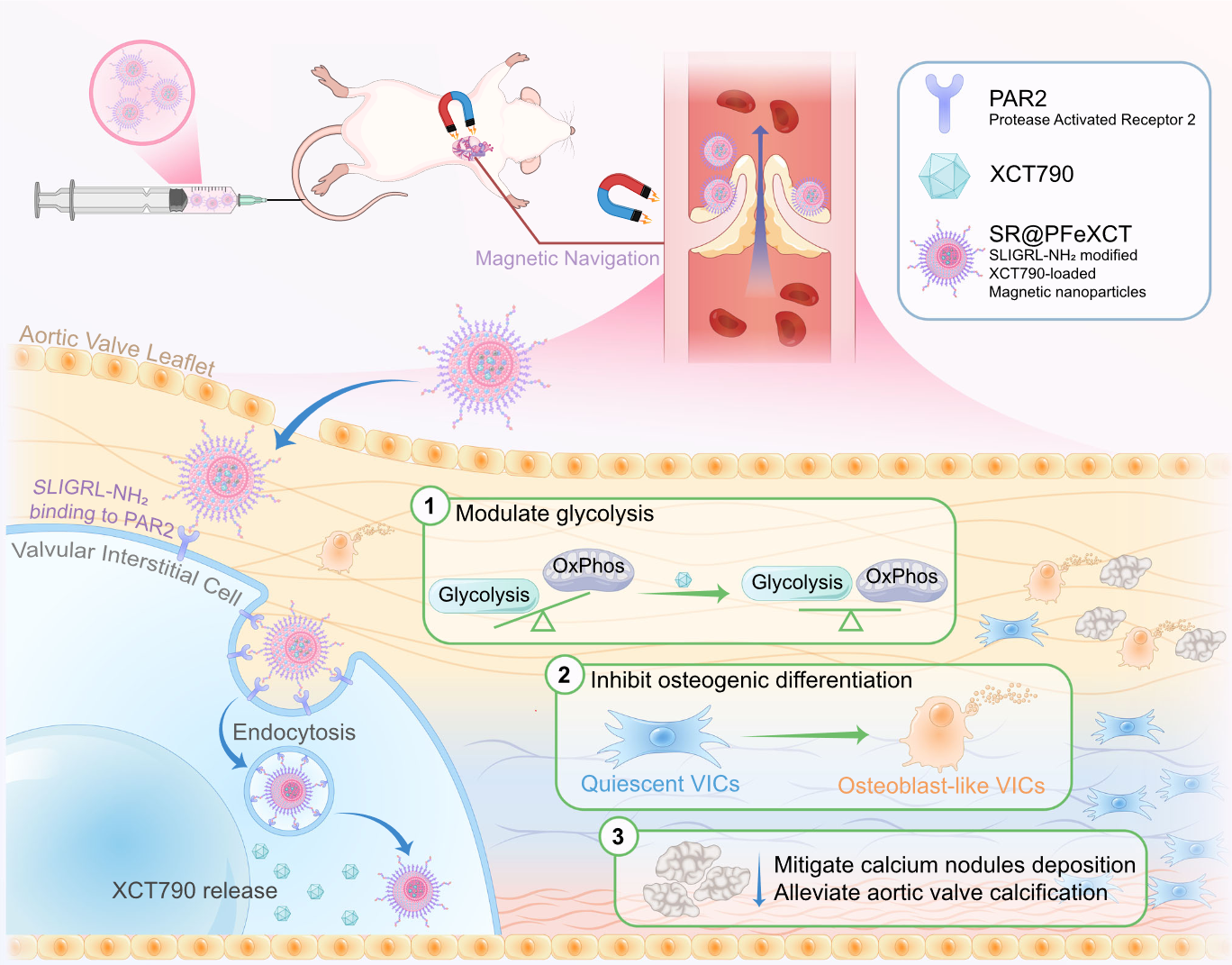
创新性与启发
- 基于 PAR2 靶向 VIC 的同时还做了磁场引导,很好的将药物递送到成骨 VICs,并且选择了激活后会被内吞的 PAR2 受体
- 磁场将纳米颗粒富集到心脏区域 — 纳米颗粒表面结合的配体 PAR2 精准定位到 VIC 表面 — PAR2 受体激动后细胞内吞,药物进入胞内
- 物理与生物医学的结合
- 多组学分析的手段
可能存在的局限性?
- 关于细胞水平研究:
- 未能使用小鼠 VIC 进行研究,以便与小鼠模型进行匹配。
- 本研究中细胞水平的研究除了使用人 VIC 外,还使用了小鼠 MOVAS-1 细胞系,该细胞系为 VSMC,尽管其与 VIC 有相似之处,但不完全一样。
- 关于小鼠 cavd 模型:
- 在验证 PAR2 在 cavd 中高表达时,使用了 Ldlr+HFD(高脂模型)以及导丝损伤双模型
- 然而在后续的疗法干预实验中,仅使用了高脂模型。
- 个人推测:是否因为作者后续的探索的 XCT790 下游机制设计到糖代谢,而与高脂模型相比,导丝损伤模型在代谢重编程方面并不明显?
- 作者在引文中强调,纳米颗粒的靶向作用,能够减少药物的全身效应。XCT790 作为影响代谢的药物,甚至可以导致 NASH,那么纳米粒子包裹后其对小鼠全身代谢的影响如何?有没有必要进行验证?
本研究通过靶向PAR2的磁性纳米颗粒,实现了针对主动脉瓣钙化的靶向药物递送系统。研究发现PAR2在成骨细胞中高表达,并促进瓣膜钙化,针对PAR2阳性细胞的干预可抑制瓣膜钙化的发展。利用功能化的纳米颗粒成功提高了与细胞的结合力,为针对CAVD的治疗提供了新思路。
© 版权声明
文章版权归作者所有,转载请注明来源。
THE END






暂无评论内容