EHJ:Lumican通过H3组蛋白乳酸化促进CAVD
Title: Lumican promotes calcific aortic valve disease through H3 histone lactylation
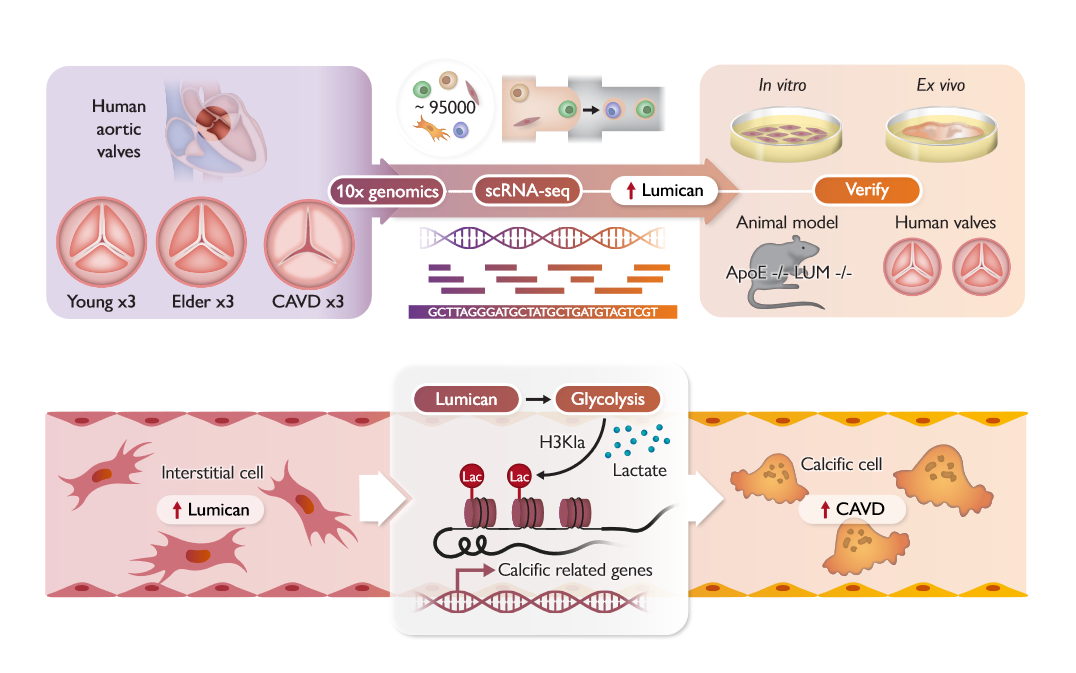
引文
1. CAVD的背景与临床挑战
- 高发病率和高致病率:CAVD是一种常见的心血管疾病,具有较高的发病率和致病率。
- 缺乏有效药物干预:目前尚无有效的药物能够阻止或减缓CAVD的发展。当CAVD发展到严重阶段时,唯一有效的治疗手段是外科手术更换瓣膜,但手术往往伴随着并发症,且长期预后不佳。
2. 研究的紧迫性
- 机制不明:尽管有许多研究试图揭示CAVD的病理过程,但其主要调控因子和具体分子机制仍不清楚。
- VICs的作用:现有的研究表明,瓣膜间质细胞(VICs)在各种因素的刺激下获得钙化特性,表达关键的骨生成标志物,这对于主动脉瓣钙化的启动和进展至关重要。
3. 单细胞RNA测序的应用
- 研究发现的复杂性:最近的单细胞RNA测序(scRNA-seq)研究揭示,VICs的骨生成转变比之前所认为的更加复杂。VICs首先产生多种过渡状态的细胞亚群,然后转变为骨生成表型的细胞亚群,从而启动瓣膜钙化。
- 未知的信号机制:尽管已有研究揭示了这一复杂转变,但具体的信号机制仍不明确。
4. 研究目的
- 扩大研究样本:为推进前期工作,研究团队进一步对来自不同年龄组(年轻、年老和钙化患者)的主动脉瓣样本进行scRNA-seq分析,以阐明可能导致钙化的VICs病理转变,并确定这一过程中涉及的关键因素。
- 发现LUM的关键作用:通过scRNA-seq数据,研究团队成功地描述了VICs病理转变的阶段,并突出了LUM(Lumican)在CAVD中的重要性。LUM是一个普遍存在的细胞外基质(ECM)成分,被认为在多种组织的纤维化和钙化病变中起重要作用。
5. LUM在CAVD中的潜在机制
- LUM的多重作用:已有大量研究表明LUM与炎症性疾病和动脉粥样硬化密切相关,这些疾病的病因与CAVD类似。虽然LUM诱导组织钙化的机制已在其他组织中得到研究,但其在瓣膜钙化中的具体作用尚未得到探索。
- 研究目的与方法:本研究旨在通过多组学方法,揭示LUM在瓣膜钙化中的作用及其潜在的分子机制。
- 主要发现:研究结果表明,LUM的升高有助于炎症反应的启动和通过糖酵解生成乳酸,这两者均与钙化有关。此外,LUM还在H3组蛋白的乳酰化修饰中发挥了此前未被识别的作用,这对于目标基因的捕获至关重要。更重要的是,LUM的去除导致乳酰化水平下降,并伴随着钙化的改善。
6. 研究的创新性和潜在应用
- LUM去除的治疗潜力:LUM的去除可能成为一种新型的CAVD治疗策略。
- 新的研究视角:这些新发现为LUM–代谢组–表观基因组在CAVD中的级联机制提供了新的研究视角。
本文的主要研究结果
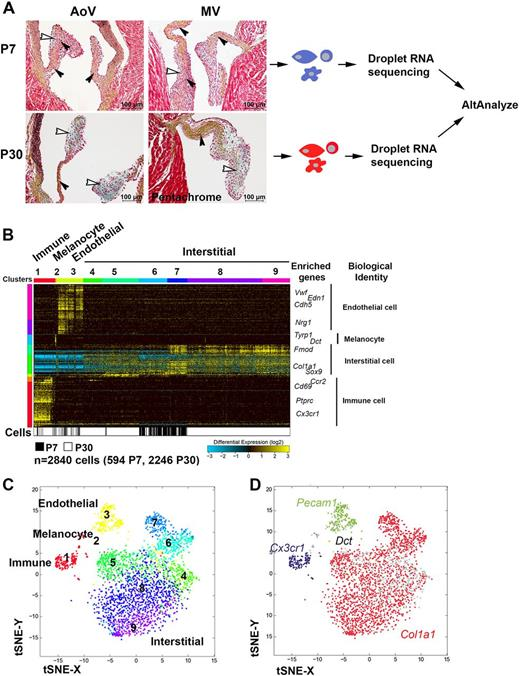
人类主动脉瓣组织的单细胞转录组景观
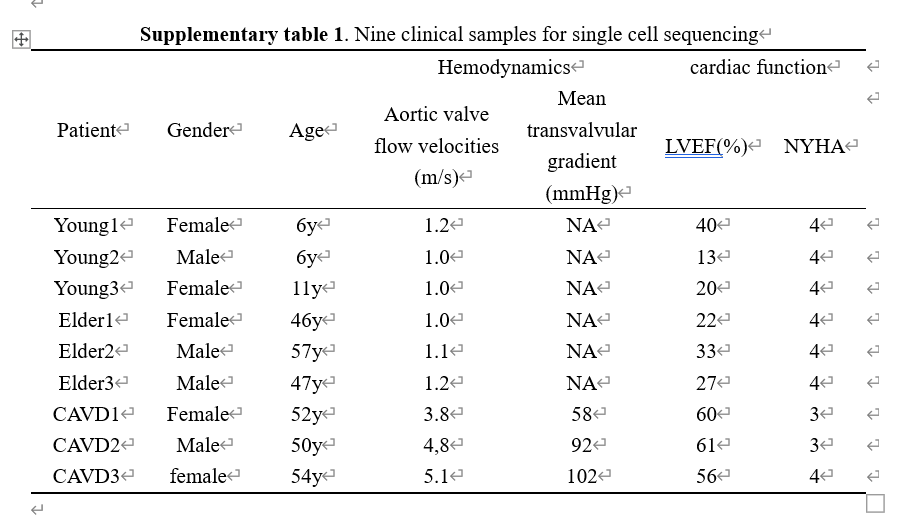
- 9个样本,分3组,共 94 277 个细胞
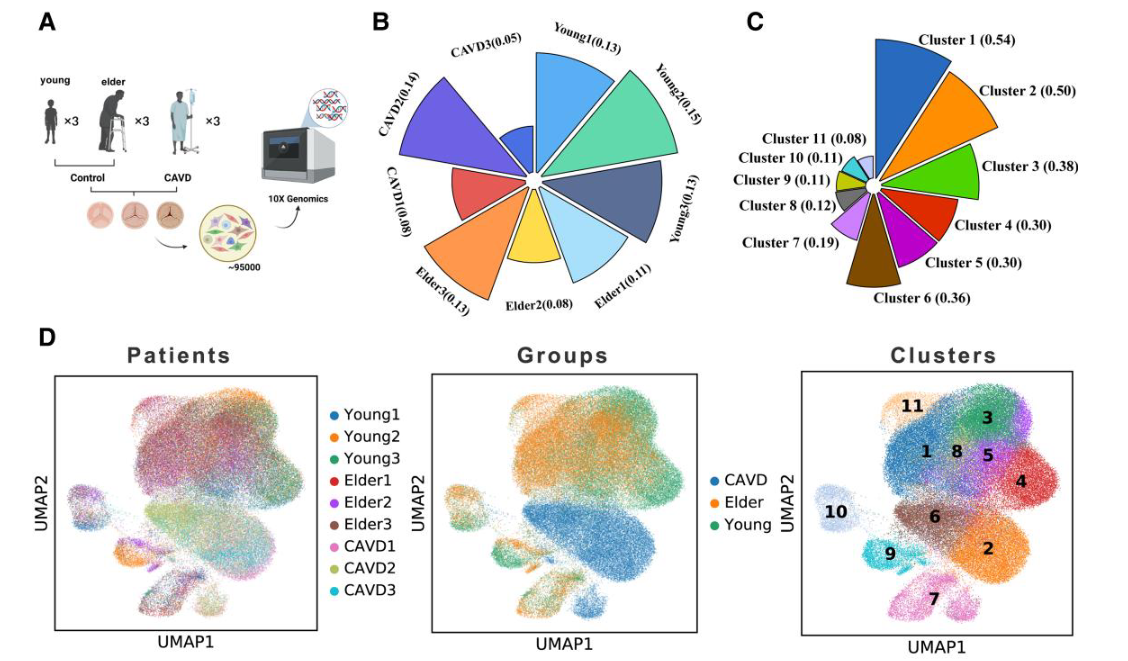
- 数据展示:所有细胞共分为11个cluster
单细胞测序发现lumican在CAVD的初始阶段发挥重要作用
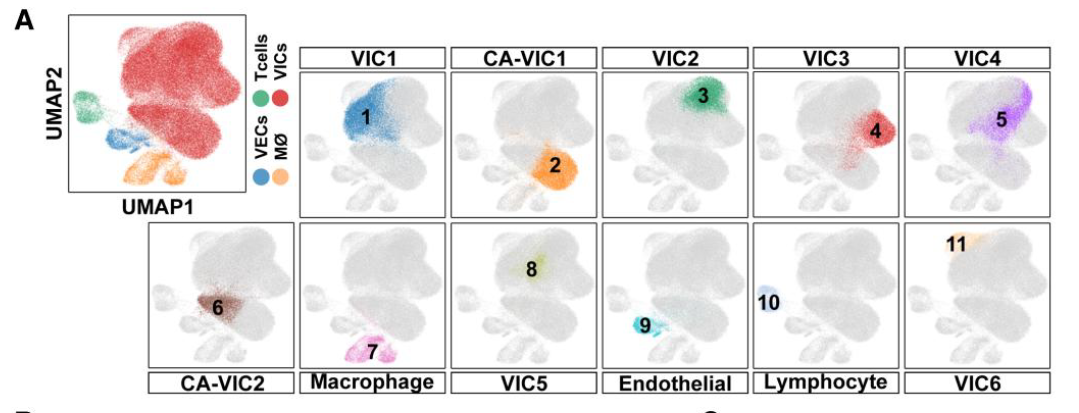
- 作者主要关注其中的VIC群体,本研究没有涉及其他细胞。
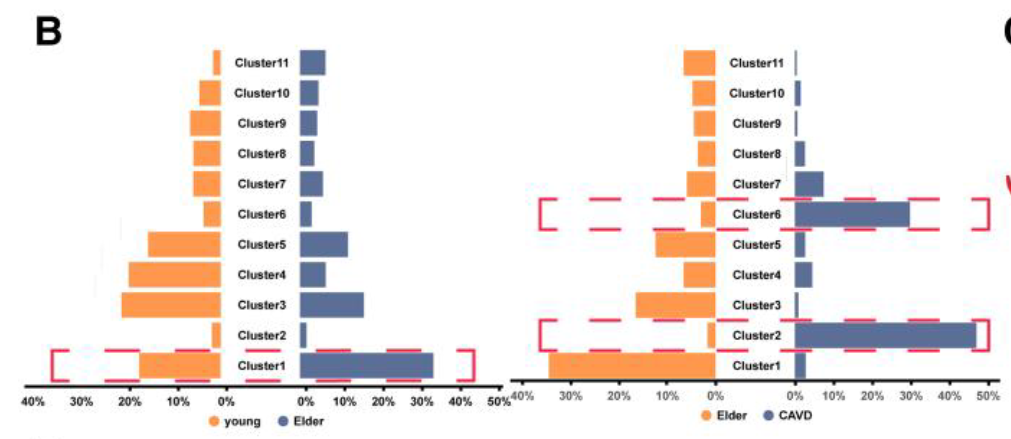
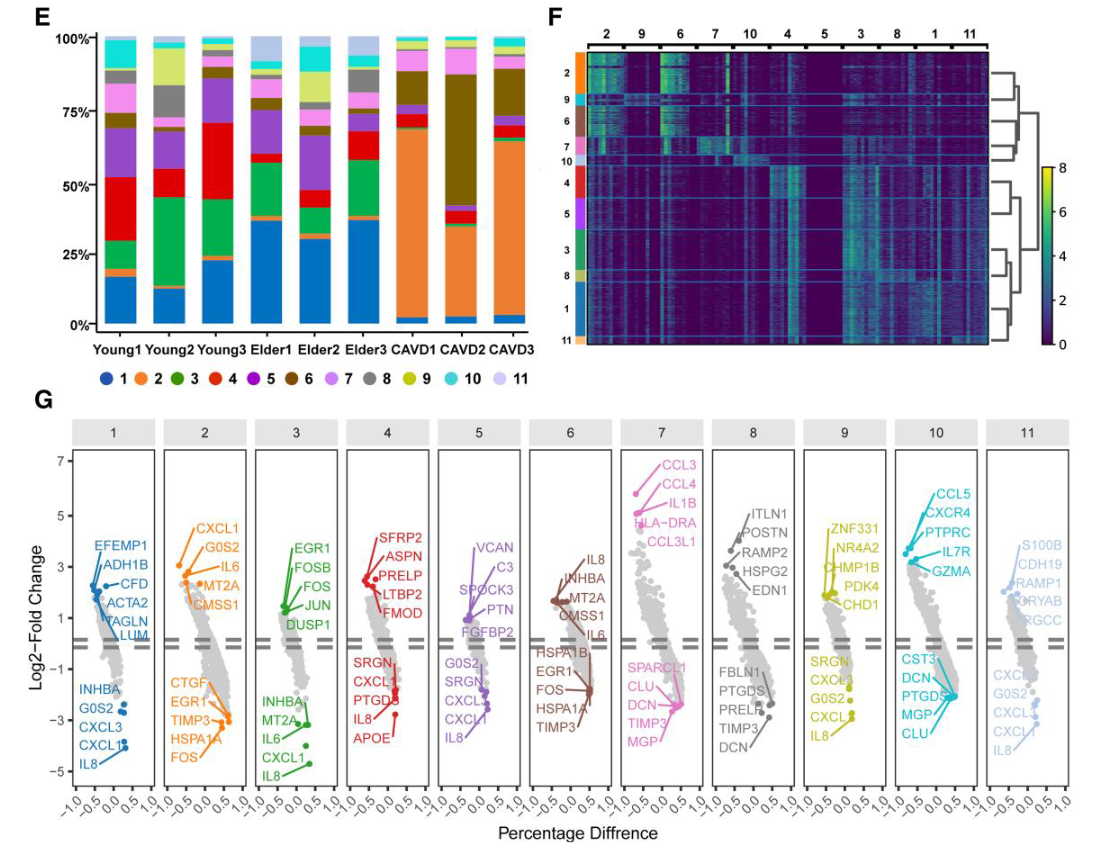
- 在年轻组中,各个VIC亚群的比例保持相对平衡,而群体1的比例显著增加,占总细胞的34.5%,并成为老年组瓣膜间质细胞的主要组成部分。
- 在CAVD组中,2和6成为主要亚群,总共占据77%的细胞,因此将它们指定为CA-VICs。
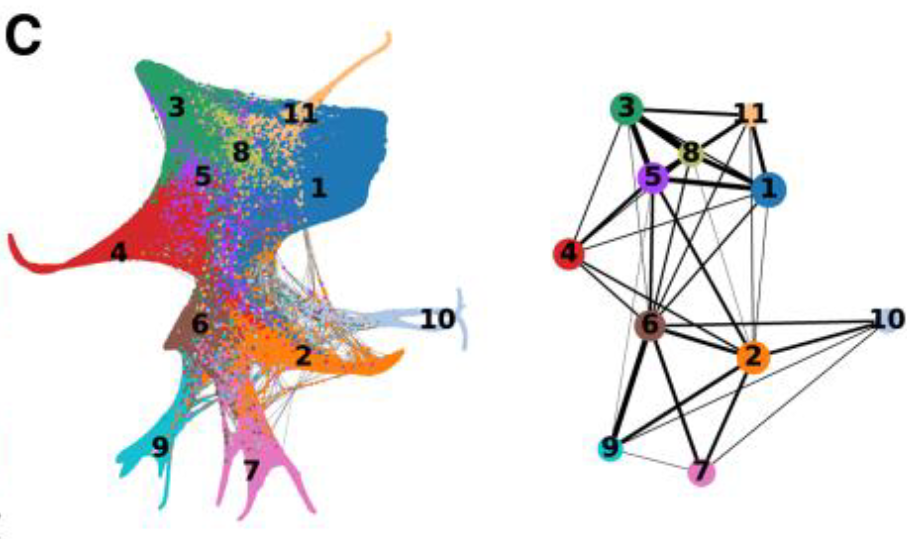
- PAGA分析表明,簇1与VIC组中的其他簇具有相互转换关系,并且与CA-VICs的位置似乎更接近。
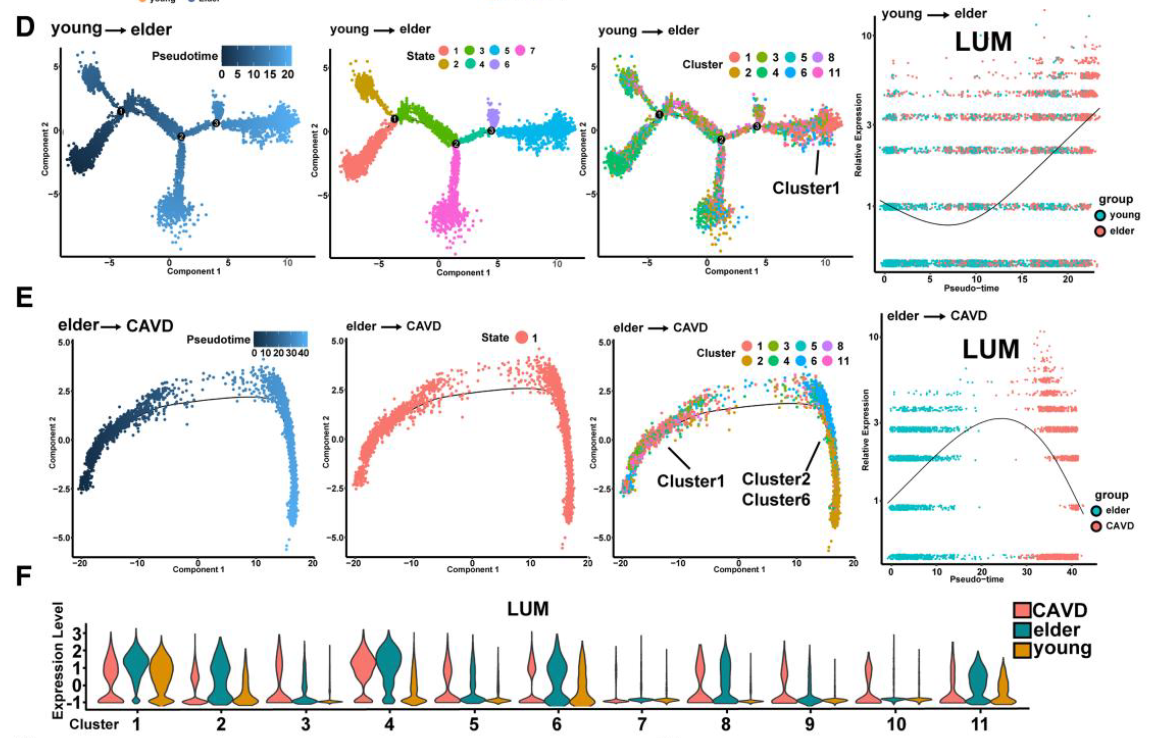
- 2次伪时间分化轨迹分析:从年轻组到老年组的过渡,以及从老年组到CAVD组的过渡。
- 在第一阶段,大多数Cluster 1细胞位于分化的末端,并且这些细胞中的特征基因LUM显著上调。
- 在CAVD疾病的发展过程中,主要的细胞演变涉及Cluster1细胞转化为CA-VICs,且LUM基因的上调在这个过程中持续存在。
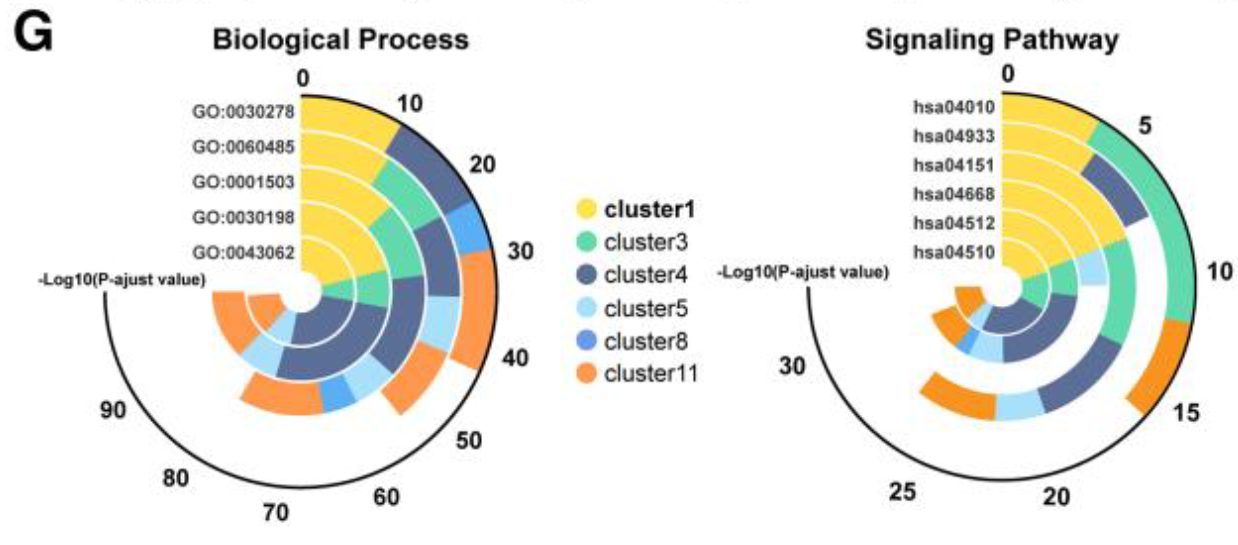
- 富集分析显示:VIC(六个簇)细胞具有相似的生物功能,前五个功能分别为细胞外结构组织、细胞外基质组织、骨化、间充质发育和骨化调节。
- 簇1 VIC 的以上五个功能中均比较突出
- Focal adhesion, ECM–receptor interaction, tumor necrosis factor (TNF) signaling pathway, PI3K-Akt signaling pathway, AGE-RAGE signaling pathway, and MAPK signaling pathway 在这些过程中发挥了重要作用
- 在CA-VICs(簇2和6)中进行了GO和KEGG分析,并显示出在调节细胞形态发生、细胞外基质组织和
组蛋白修饰方面的活跃生物功能。
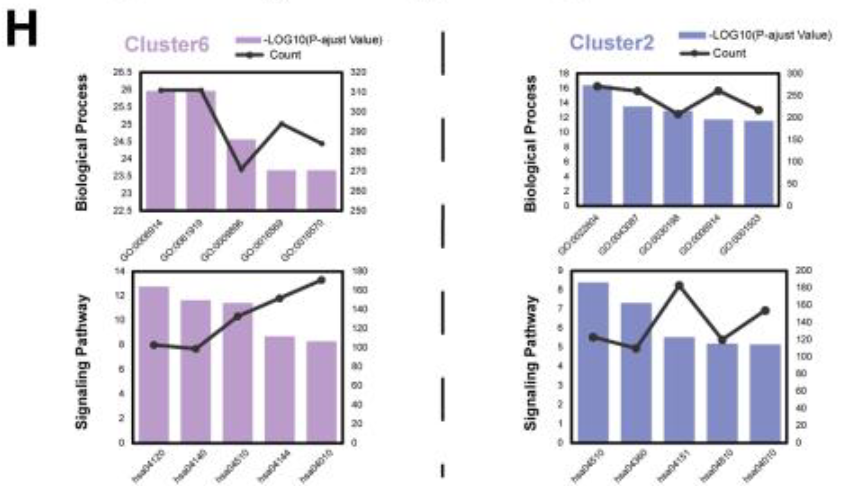
- 对各种组样本进行的KEGG分析显示,
组蛋白修饰在CAVD组中表现出显著影响。根据上述分析,可以推断集群1在CAVD的初始阶段发挥着关键作用,其独特基因LUM可能作为其功能的关键决定因素。
验证lumican与CAVD之间的相关性
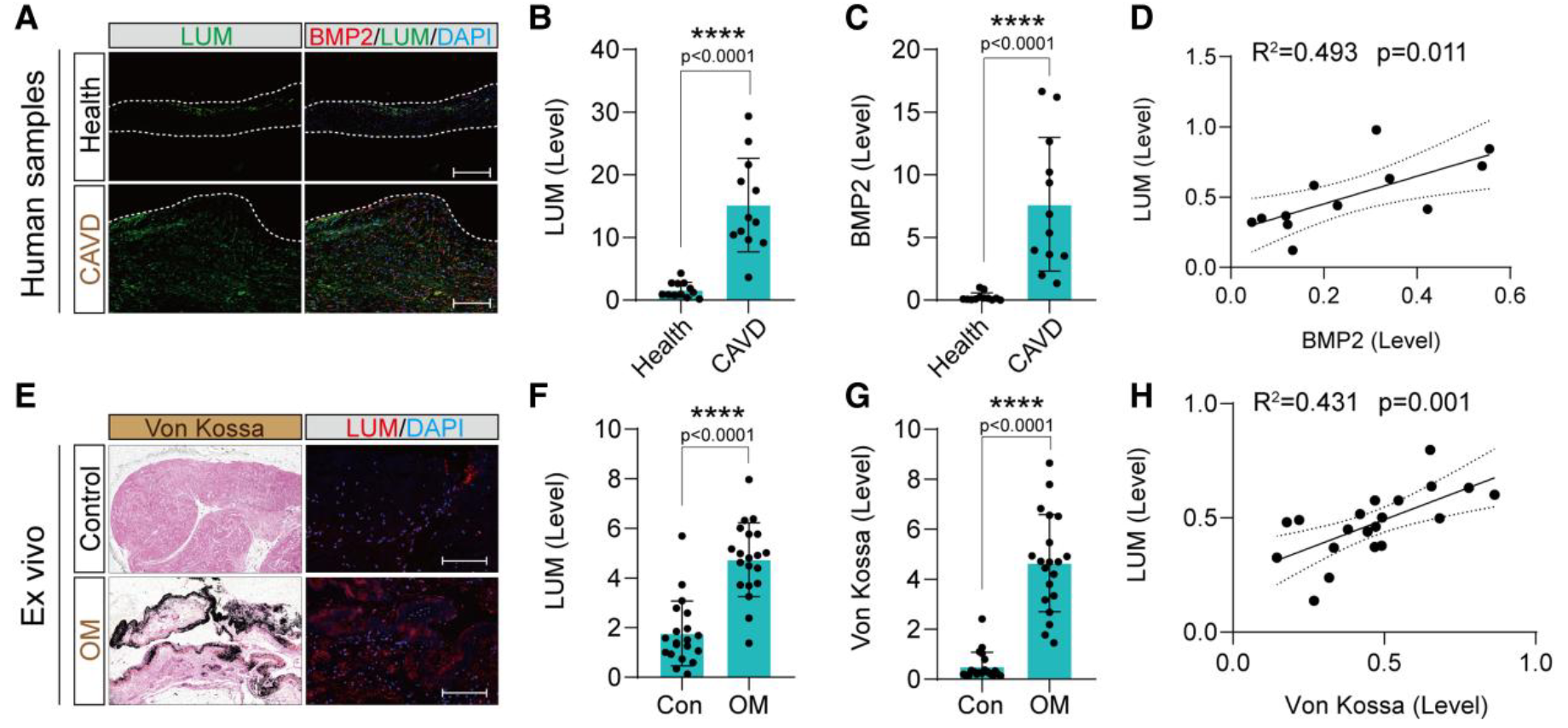
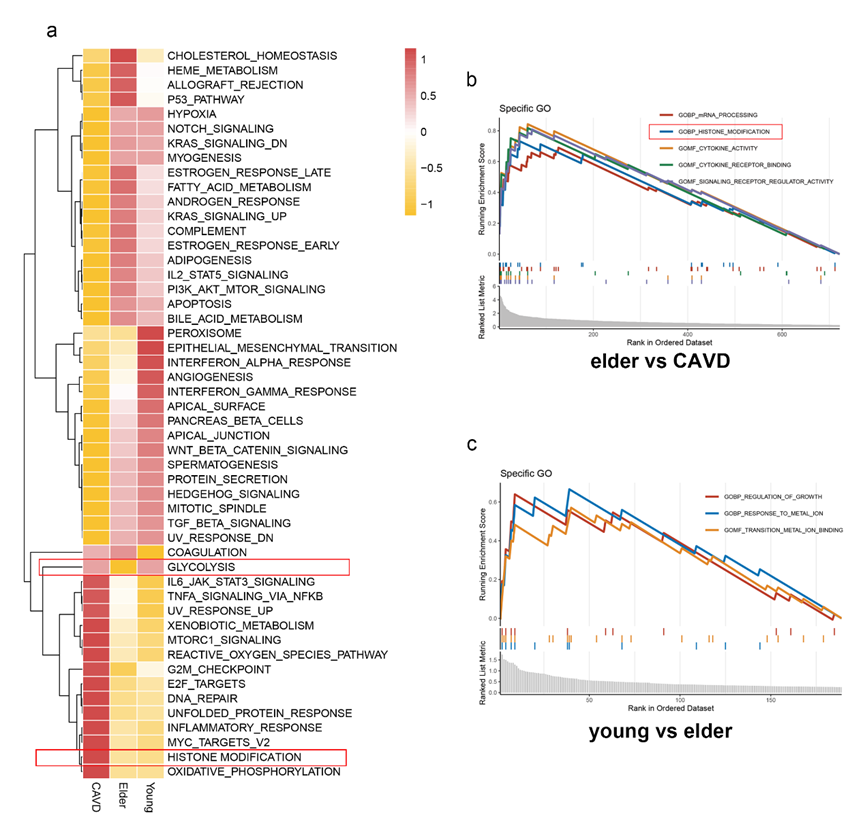
- 人类样本验证
- LUM 与 BPM2 正相关
- LUM 与 钙染色正相关
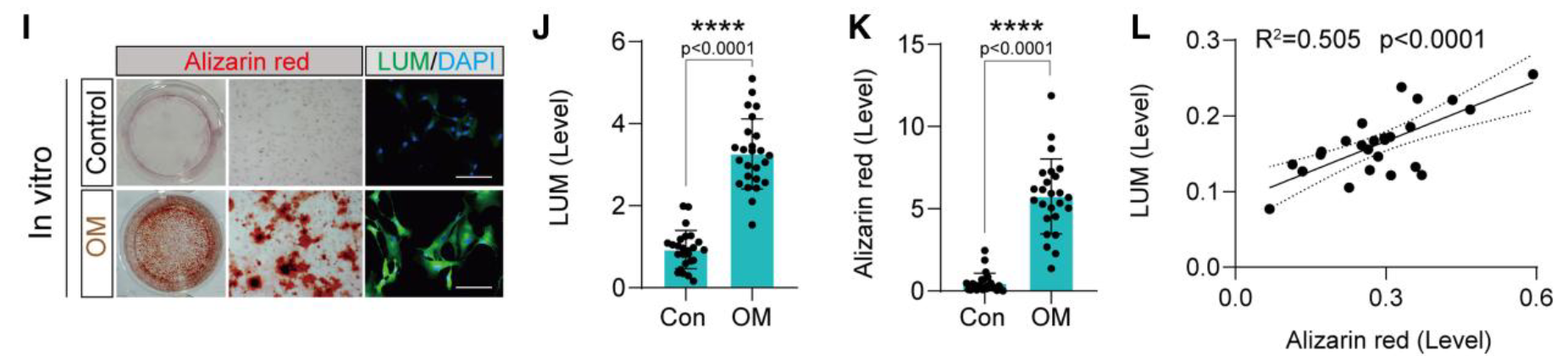
- 人VIC验证
- OM组LUM升高,与茜素红正相关
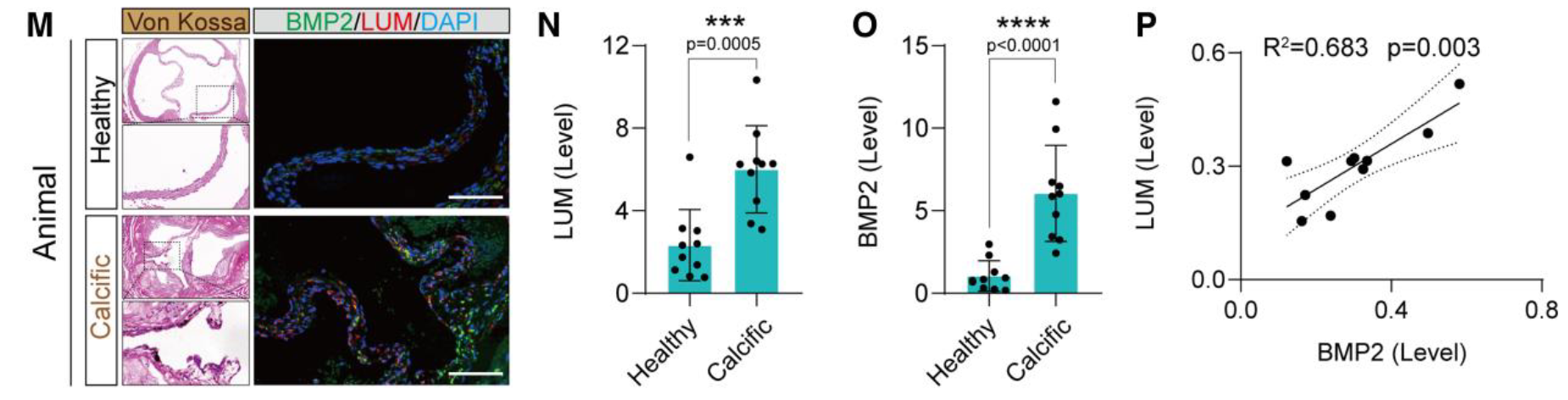
- 小鼠模型验证(ApoE−/− 高脂喂养6月)
- LUM与小鼠瓣膜钙化水平正相关
Lumican 促进主动脉瓣钙化
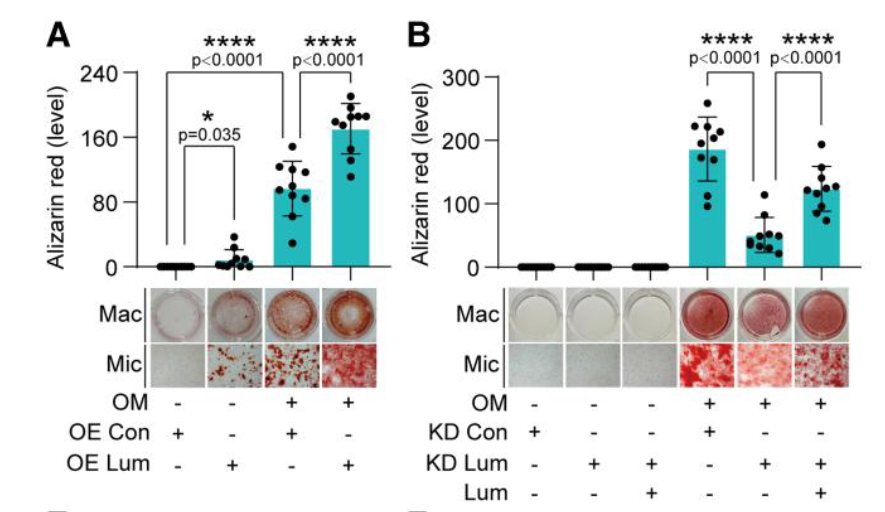
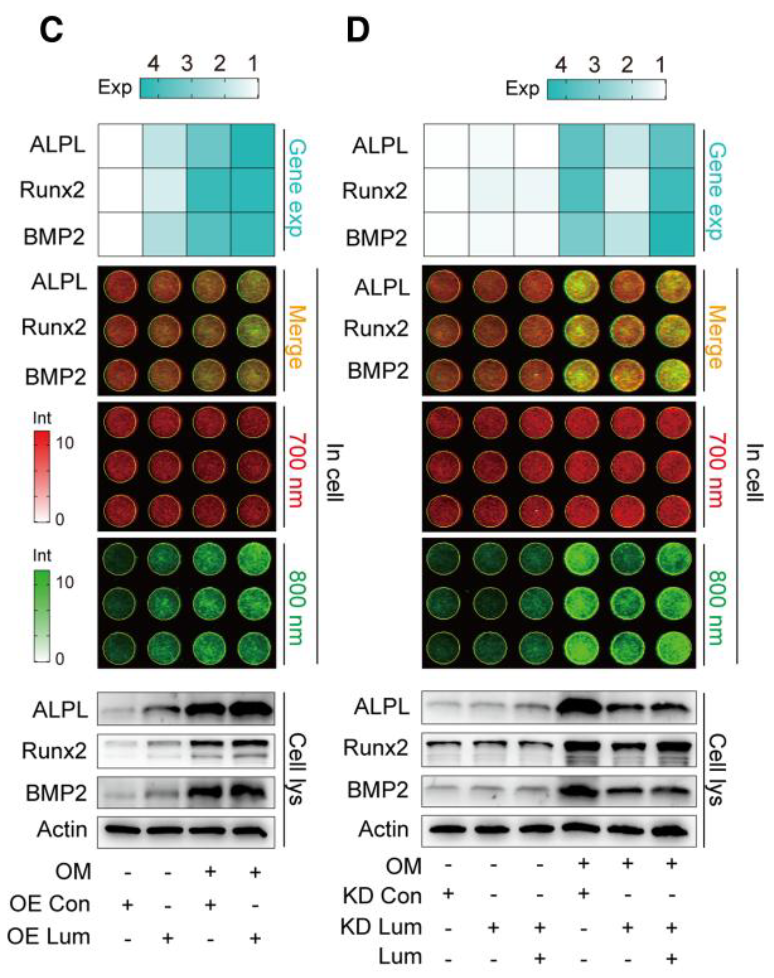
- In vitro 细胞水平,LUM过表达(OE)可以促进VIC钙化,而敲低(KD)延缓钙化
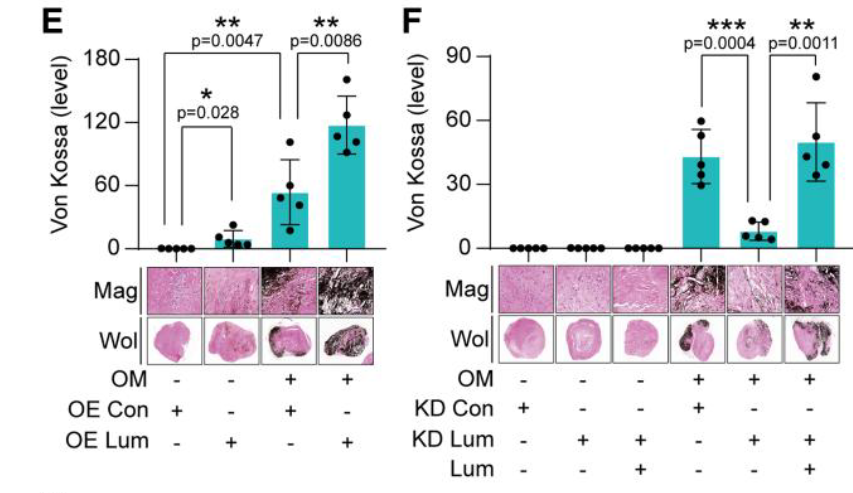
- ex vivo:实际上是组织块培养法
- 与细胞水平结论相同
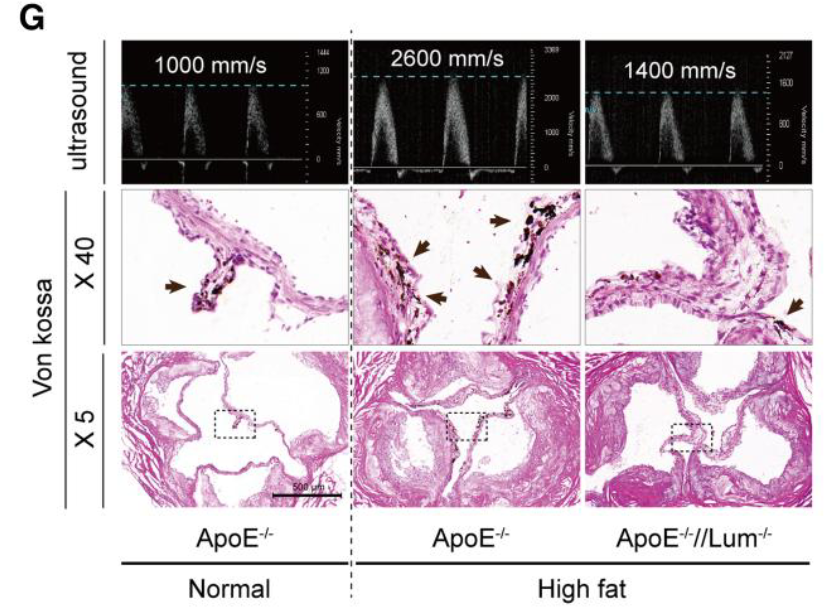
- 小鼠模型中LUM/APO双敲除组流速较APO组明显下降
lumican 促进钙化作用与糖酵解相关
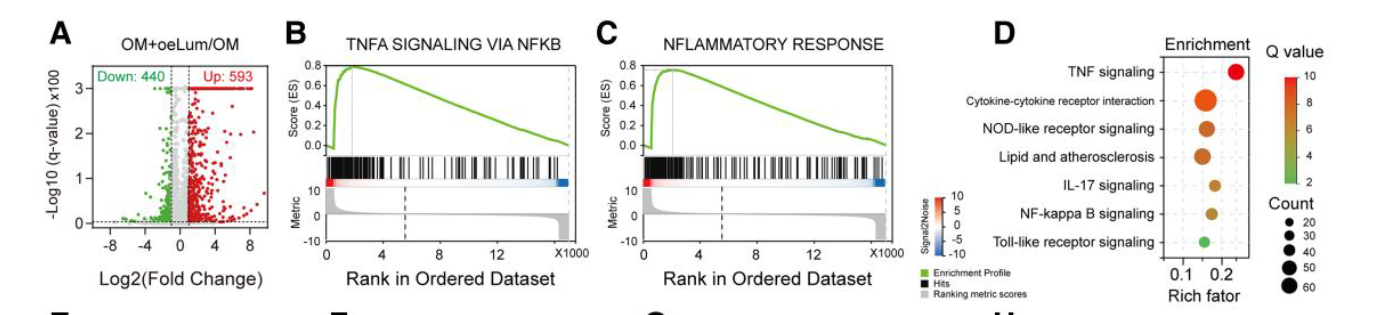
- 体外细胞培养的转录组分析
- TNF NFKB
- KEGG:TNF信号通路、细胞因子-细胞因子受体相互作用和NOD样受体信号传导作为与LUM介导的效应相关的前三个最活跃的信号通路
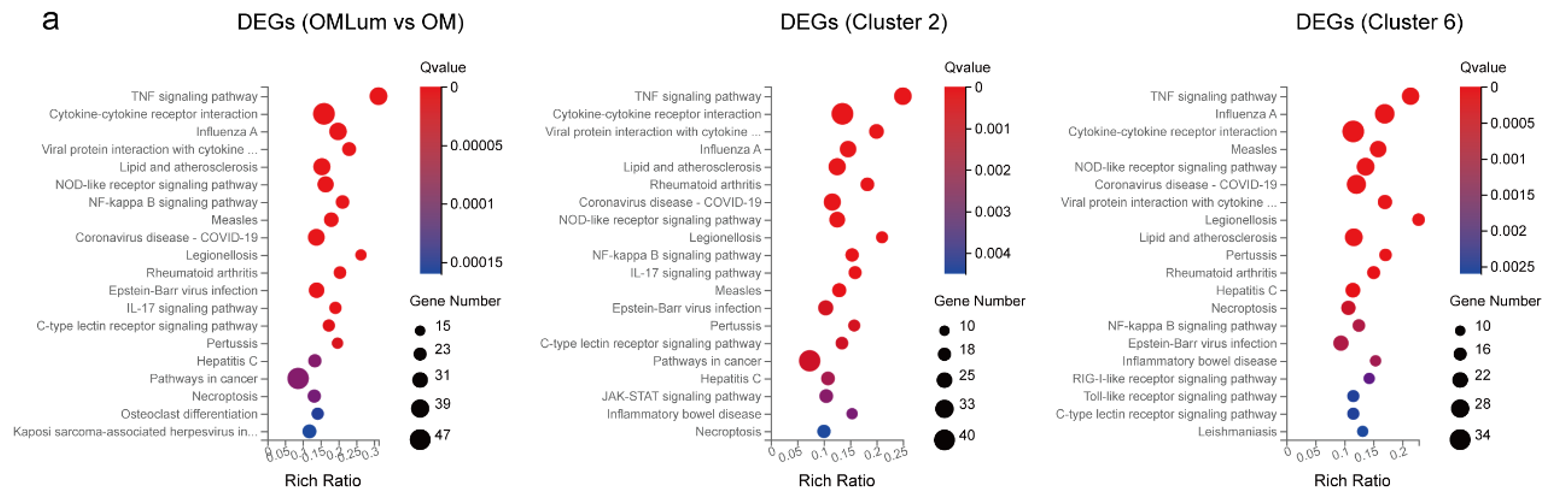
- 这些通路与单细胞分析中C2 C6亚群的富集通路非常相似
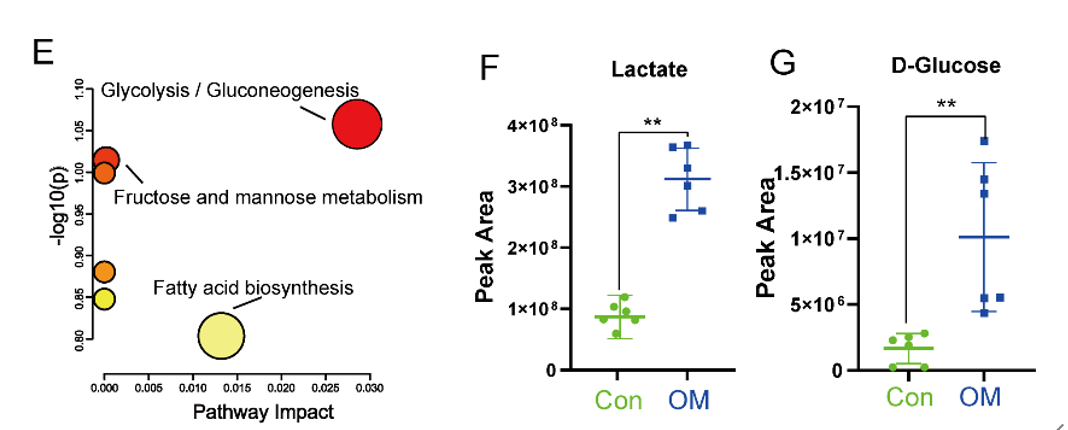
- 代谢组分析发现
- OM诱导的VICs细胞乳酸和葡萄糖的产生增强,而差异代谢物主要富集在糖酵解/糖异生途径中
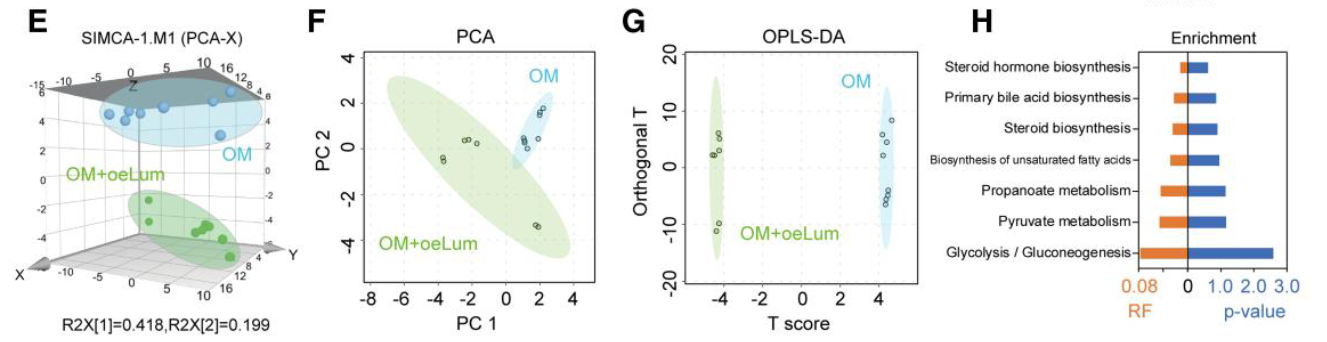
- Lum处理的代谢组也发现了糖酵解途径的激活
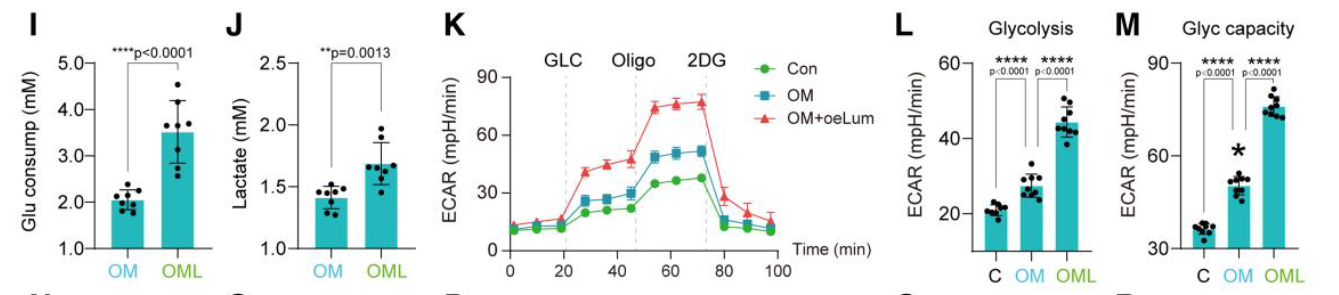
- 细胞培养发现添加LUM 葡萄糖和乳酸的生成增加
- ECAR实验发现糖酵解火星增强
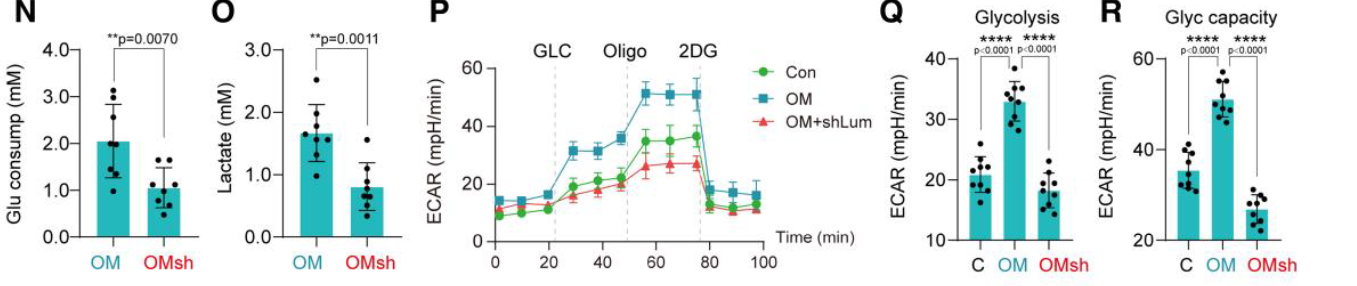
- 细胞水平敲低lum之后,结果与上述相反
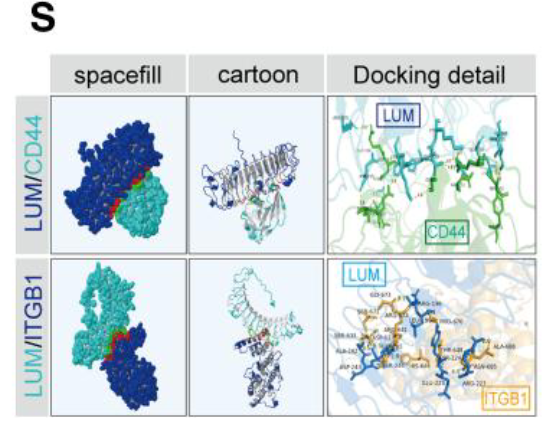
分子对接分析的结果表明,LUM 对 CD44 和 ITGB1 受体均具有亲和力,分子结合能分别为 -5.9 kcal/mol 和 -3.3 kcal/mol。(对CD44的亲和力更强)
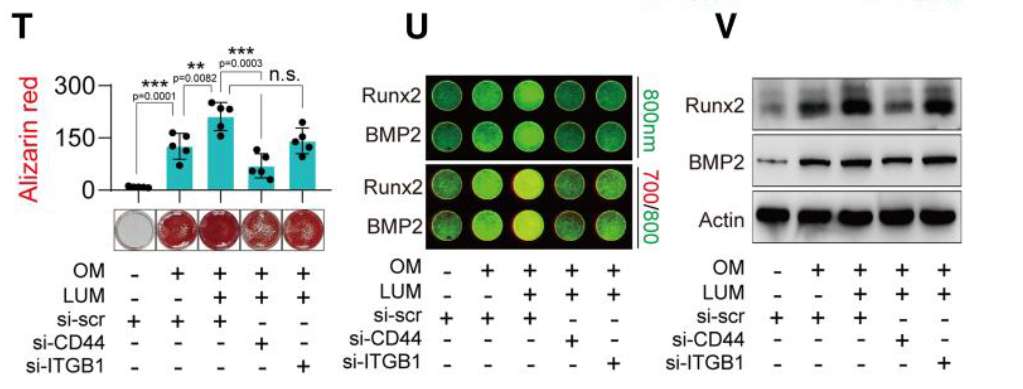
- 细胞水平再次验证,敲低CD44 和 ITGB1
- 敲低CD44之后,LUM的促进钙化能力显著下降
- 表明LUM的促钙化作用需要通过CD44介导
Lumican 也参与了与 H3 组蛋白乳酸化相关的瓣膜钙化
(既往研究已经证明乳酸化在糖酵解中发挥作用)
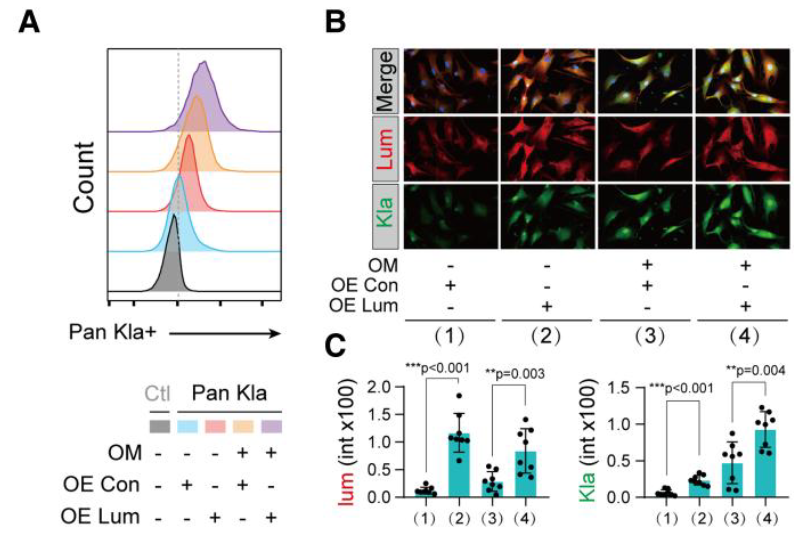
流式细胞术分析显示在OM诱导后,整体乳酸化水平显著增加。OM刺激和LUM应用的结合产生了增强的效果,使OM组中观察到的乳酸化水平几乎翻倍。(KIa是总体乳酸化标记物)
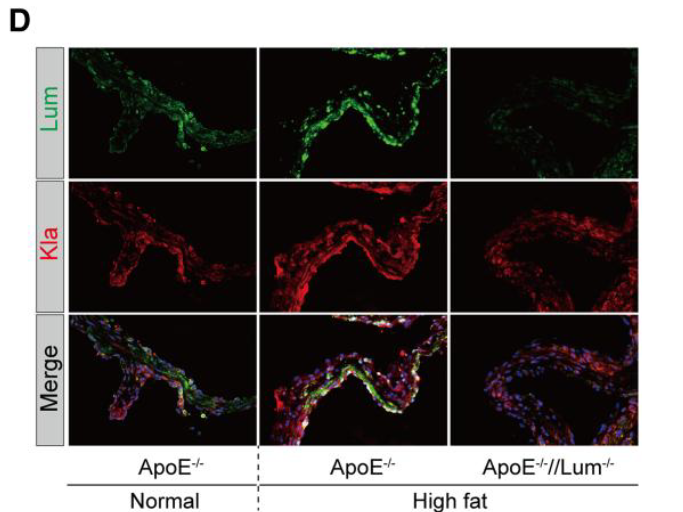
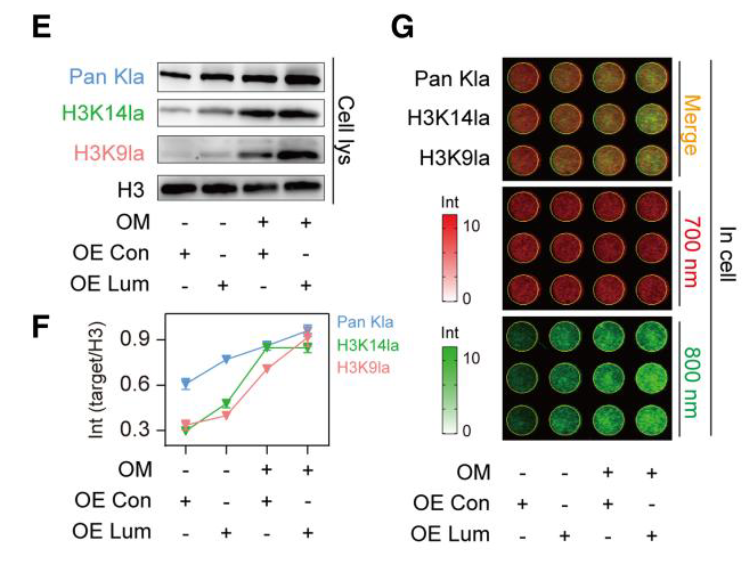
- OM刺激对H3K9la和H3K14la的表达具有显著影响
- 而添加LUM之后进一步增强
- in cell分析发现在LUM过表达的情况下,H3K9la和H3K14la表达的上调与BMP2一致
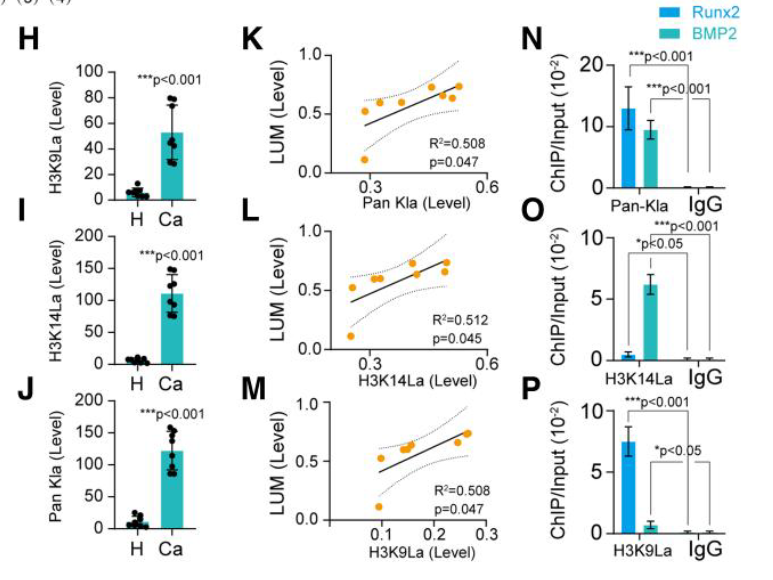
- 组织标本检测结果(H I J )
- 此外,LUM的表达与乳酸化水平之间,特别是H3K9la和H3K14la的共表达分析展现出线性相关性(图6K–M)。
- ChIP-PCR结果也表明组蛋白乳酸化在增强BMP2和Runx2基因转录中发挥了作用(图6N)。
- 上述结果还表明:修饰位点H3K14la调节BMP2基因(图6O),而修饰位点H3K9la调节Runx2基因(图6P)。
讨论(原文)
1. 研究背景与初步发现
- VICs转变为病理性表型:单细胞数据支持了VICs在CAVD中转变为骨生成细胞群的过程,显示在转变为最终骨生成细胞之前,VICs会经历中间状态的细胞亚群。
- LUM的关键作用:研究首次确认了LUM在这种转变过程中的重要角色,LUM被认为是从VICs向病理性表型转变的关键调节因子。
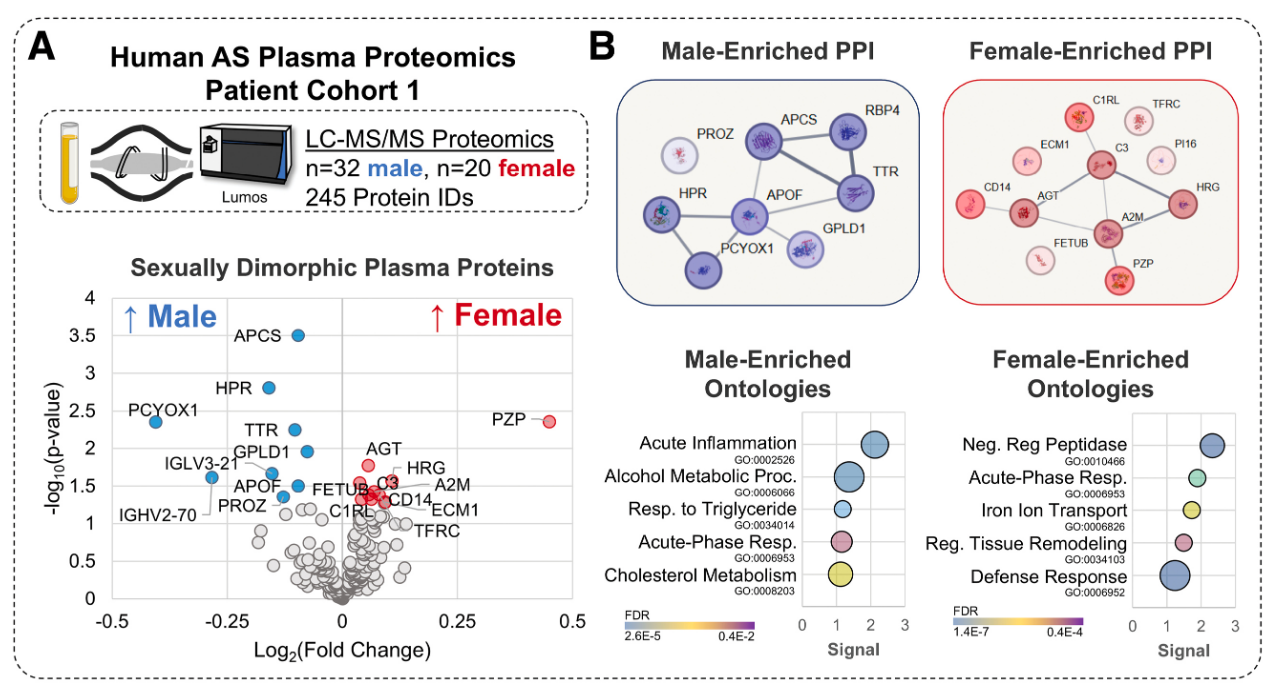
2. 性别差异的考虑
- 性别差异:尽管在分析中没有专门考虑性别差异,但研究中包括了男性和女性样本,以减少潜在的性别相关差异对结果的影响。
3. LUM在CAVD中的作用
- LUM和骨生成:研究发现,LUM与骨生成标志物(如ALP、Runx2、BMP2)的表达呈正相关,LUM沉默导致这些标志物表达下降,并减少了钙沉积。
- 动物模型验证:ApoE−/−//Lum−/−双基因敲除小鼠的实验显示,LUM缺失改善了钙化、组织结构和血流情况。
4. LUM的炎症调节作用
- 炎症反应:LUM通过促进TLR4的富集,提升了炎症反应,这种现象在CAVD和败血症模型中均有观察到。
- 与代谢调节的关系:LUM在钙化病变中还通过促进糖酵解和乳酸生成来调节代谢,这表明LUM可能在组织纤维化和钙化中扮演了此前未被识别的角色。
5. 表观遗传调控
- 组蛋白乳酰化:LUM还参与了H3组蛋白的乳酰化修饰,促进了骨生成基因(如Runx2和BMP2)的转录,这进一步增加了钙化潜力。
- LUM的复合调控作用:LUM不仅直接调控炎症反应,还通过表观遗传修饰增强病理条件下的钙化潜力。
6. LUM与CD44的相互作用
- LUM与CD44:LUM可能通过与CD44相互作用来调节糖酵解,进而影响主动脉瓣的钙化过程。
7. 研究的局限性
- 样本量与选择偏倚:研究样本量较小,可能引入选择偏倚,且未充分考虑性别差异对结果的影响。
- 模型局限性:所使用的高脂饮食喂养ApoE−/−小鼠模型可能不完全反映CAVD的复杂病理过程,需要进一步研究LUM在其他动物模型中的作用。
- 长期影响的缺乏:随访时间较短,无法充分展示LUM沉默对CAVD长期影响,需要更长期的研究验证。
8. 未来研究方向
- LUM上游信号通路:进一步研究LUM在CAVD中的上游信号通路可能有助于全面理解其在病理过程中的作用。
- 多层次干预策略:针对LUM的干预策略可能在多个层次上阻断CAVD的病理级联反应。
讨论(我的)
逻辑梳理
- VICs哪个亚群发挥了促进钙化的作用?单细胞分析获得CA-VICs
- 关键基因如何锁定?多种分析方式联合发现LUM的潜在作用
- LUM 与CAVD的相关性证明(组织、细胞、组织块、小鼠)
- LUM 与CAVD的因果关系证明
- 下游机制探讨1:转录组与代谢组联合分析锁定糖酵解代谢差异
- 下游机制探讨2:乳酸化通路验证
- 下游机制探讨3:LUM作为一个分泌蛋白,其受体的检测
- 下游机制探讨4:乳酸化的靶点鉴定
我们可以借鉴的一些方法
- In cell WB实验
- 多组学分析的思路
- 组织块培养的方法 ex vivo
- 分子对接作为分子相互作用的参考
本研究可能存在的一些局限性
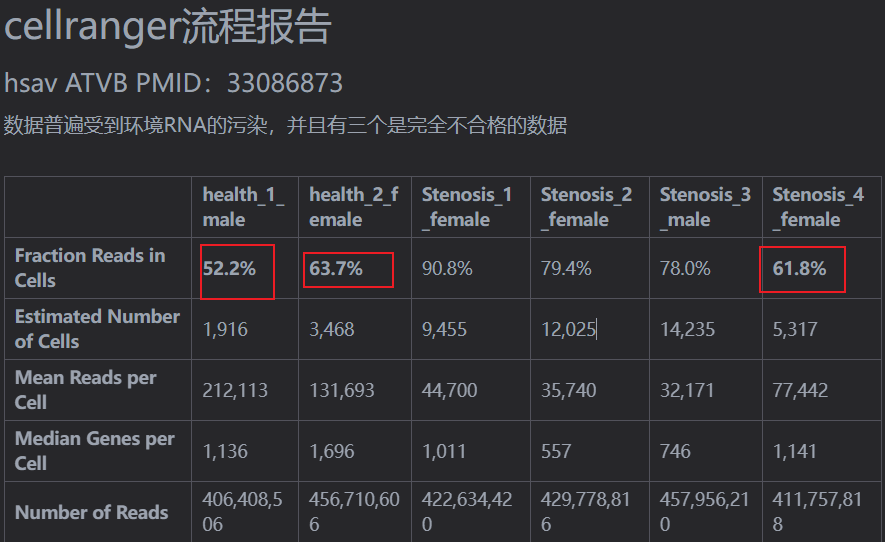
- 单细胞数据的样本差异非常大,但是文章中没有进行批次效应的矫正,这不是常规的实践流程


- 单细胞数据中,LUM的表达实际上在CAVD样本中是相对下降的,而不是一直升高,与文中说的不完全一致
- 分子对接部分实际上是计算模拟,使用免疫共沉淀进一步验证会更严谨
- 如何锁定到组蛋白修饰的位点这部分不够清晰
Ex vivo calcific culturing
Five human aortic valve leaflets were cut into 1-mm3 sections and treated with oe and ko of LUM and LUM factor supplement under the condition of OM induction for 18 days. After that, the ex vivo tissues were fixed with 4% PFA for 30 min, then embedded in paraffin to make 5-μm-thick sections. The specimens were stained with von kossa. The captured images were semi-quantitated using ImageJ software. The 5 repeats were selected for statistical analysis.
本研究探讨了Lumican(LUM)在钙化主动脉瓣病(CAVD)中的作用。通过单细胞RNA测序分析发现,LUM在VICs的转变中发挥关键作用,并促进H3组蛋白乳酸化,进而加速钙化过程。去除LUM可改善钙化情况,提示其作为新治疗靶点的潜力。




- 最新
- 最热
只看作者