标题: Multitrait analyses identify genetic variants associated with aortic valve function and aortic stenosis risk
期刊:nature genetics
部分名词对照
| 专有名词 (中英文) | 在本研究中的定义与作用 |
|---|---|
| 定量内表型(Quantitative Endophenotypes) | 介于基因变异与临床疾病(主动脉瓣狭窄)之间的可量化中间特征。本研究利用深度学习从影像中提取的主动脉瓣面积、峰值流速等均属于此类,其遗传挖掘效率远高于直接分析疾病诊断。 |
| 全基因组关联分析 (GWAS) (Genome-Wide Association Study) | 一种通过扫描全基因组范围内的遗传变异,寻找与特定性状(如瓣膜流速)或疾病(如主动脉瓣狭窄)相关的遗传位点的方法。 |
| MTAG(Multitrait Analysis of GWAS) | 多性状全基因组关联分析。一种统计学方法,通过联合分析多个相关的性状(本研究中为三个瓣膜功能指标和疾病诊断数据)来提高发现新遗传位点的效能。 |
| 多基因评分 (PGS/PRS) (Polygenic Score/Risk Score) | 基于成千上万个遗传变异计算出的个体化数值,用于预测一个人患主动脉瓣狭窄的遗传风险。 |
| 孟德尔随机化 (MR) (Mendelian Randomization) | 一种利用遗传变异作为“天然随机对照试验”的方法,用以推断危险因素(如低密度脂蛋白 LDL、血磷水平)与疾病之间是否存在因果关系。 |
| 相差心血管磁共振成像 (cMRI) (Phase-contrast cMRI) | 一种能够提供主动脉内血流速度信息的影像技术。研究者利用这种技术的数据来推算瓣膜的功能状态。 |
| 主动脉瓣面积 (AVA) (Aortic Valve Area) | 评价瓣膜狭窄程度的关键指标之一。本研究通过深度学习模型计算正向心排血量与流速时间积分(VTI)之比得出。 |
| 峰值流速 & 平均压力梯度(Peak Velocity & Mean Gradient) | 反映瓣膜狭窄严重程度的流动力学指标。流速越高、压力梯度越大,通常意味着瓣膜狭窄越严重。 |
| MAGMA | 一种计算框架,用于分析 GWAS 发现的基因是否在特定的生物通路、组织或细胞类型中富集(活跃)。 |
引言
临床背景与现状:主动脉瓣狭窄的严峻挑战
- 疾病负担: 主动脉瓣狭窄(Aortic stenosis, AS)表现为主动脉瓣口的病理性狭窄,会导致高发病率和死亡率。据统计,2017年全球受影响人数超过1200万。
- 治疗困境: 目前缺乏针对AS的预防性疗法。除了手术或经皮瓣膜置换术外,尚无公认的药物治疗手段,且这些干预措施通常仅用于重症患者。
- 遗传学研究进展: 虽然已有研究确定了与AS临床诊断相关的常见遗传变异,但目前最大规模的研究也仅发现了32个基因座。
方法论基础:定量内表型的优势
- 发现效率: 研究者指出,在健康人群中分析定量内表型(如主动脉直径、左心室射血分数)是遗传发现的强大手段。定量内表型(Quantitative Endophenotypes)是指可以量化的、与疾病相关的中间表型或生理特征。
- 样本效率对比: 引言引用了2022年和2023年的两项研究对比:一项针对8,626例病例的研究仅发现了21个基因座;而另一项仅针对38,694名UK Biobank参与者进行主动脉直径(定量内表型)研究,就发现了82个基因座,其中包括了前者发现的大部分位点。这证明了定量内表型在遗传挖掘中具有更高的样本效率。
技术基础与本研究目标
- 影像学技术: 相差心血管磁共振成像(cMRI)能够提供血流模式信息,从而推断主动脉瓣的功能和病变情况。
- 技术突破: 作者团队此前开发了一种基于深度学习的模型,能够从UK Biobank的cMRI速度编码数据中自动估算具有临床意义的主动脉瓣测量值。
- 研究核心目标: 本研究旨在利用这些由深度学习提取的cMRI主动脉血流速度特征(如峰值速度、平均压力梯度和瓣膜面积),来阐明主动脉瓣功能的遗传变异基础,并探索其与主动脉瓣狭窄(AS)风险的潜在关联。
主要研究结果
基于人工智能的大规模影像特征提取与表型化
研究的核心起点是利用 UK Biobank 中 62,902名 参与者的相差心血管磁共振成像(cMRI)原始数据。
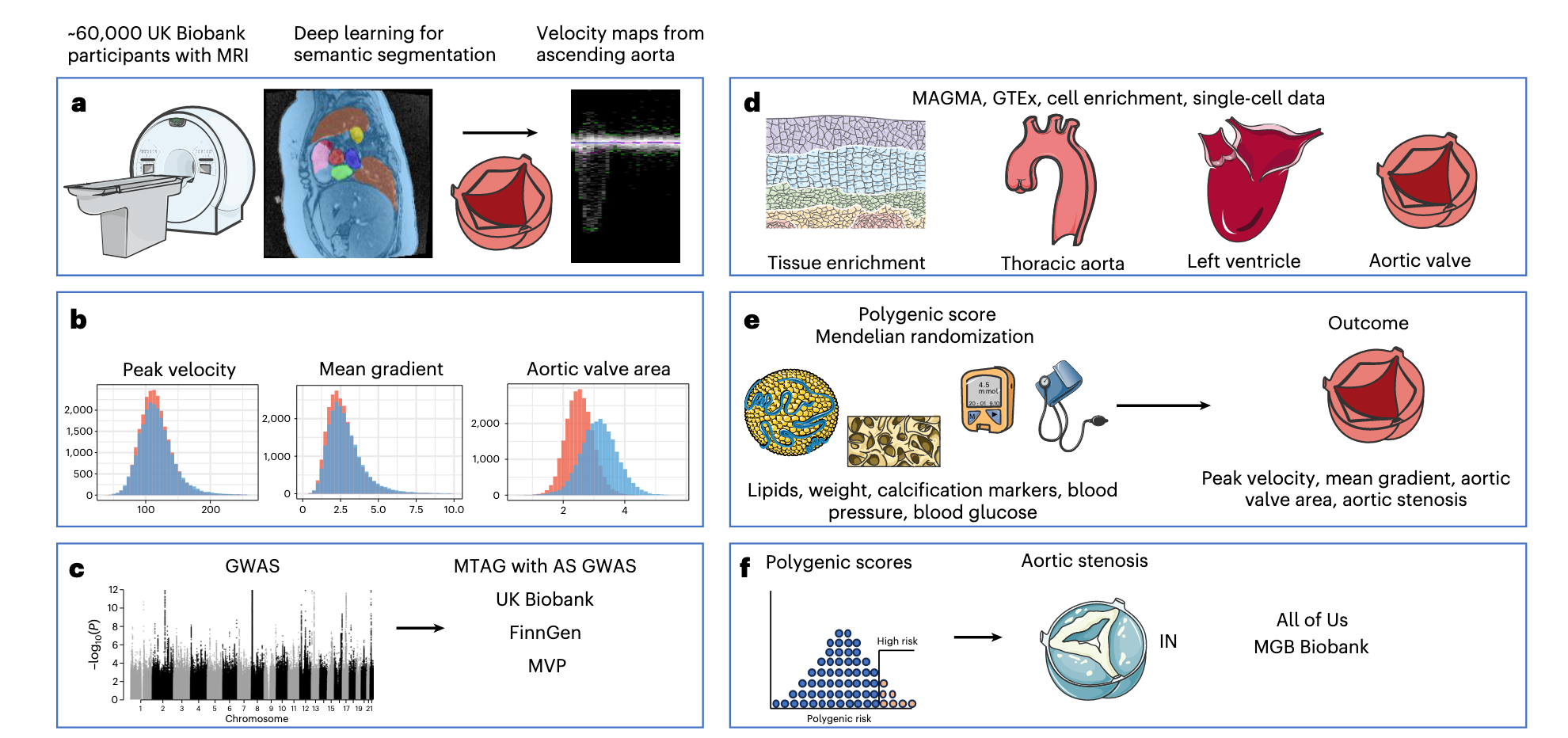
深度学习模型: 作者构建了一个基于 U-Net 架构的模型,并采用了在 ImageNet 上预训练的 ConvNext-small 编码器来提高特征识别能力。通过这一模型,研究者对升主动脉进行了自动分割(Segmentation),并从速度编码图像中提取了流速信息 (Figure 1a) 。
定量指标的计算: 基于分割掩码,研究推导出了三个关键的生理指标:
- 峰值流速 (Peak Velocity): 提取收缩期所有像素点流速的第99百分位值。
- 平均压力梯度 (Mean Gradient): 根据简化的伯努利方程 (4v2) 计算每一帧的压力差,并取收缩期的平均值。
- 主动脉瓣面积 (AVA): 通过将向前搏出量(forward stroke volume)除以流速时间积分(VTI)得出 (Figure 1b) 。
- 样本规模: 在严格剔除已有瓣膜手术、先天性心脏病及质量控制不合格的样本后,最终 59,571名 参与者进入了全基因组关联分析(GWAS)阶段。
多层次全基因组关联分析 (GWAS) 的发现
研究者首先分别对功能指标和疾病诊断进行了独立分析,随后通过整合分析扩大了发现规模。
单一性状分析 (Single-trait GWAS):
- 针对三个 cMRI 定量指标,研究鉴定出 61个 独特的遗传位点 (Supplementary Figure 2) 。
- 值得注意的是,研究发现了 X 染色体上的两个新信号:靠近 NDP(与梯度相关)和 TSPAN6(与 AVA 相关)的位点。 (Figure 2)
- 疾病元分析: 整合了来自 UK Biobank、FinnGen、Million Veteran Program 等多个队列的 4万多例 AS 患者数据,共识别出 92个 显著位点。其中包括新发现的脂质调节基因 LDLR、PCSK9 以及 SORL1。
多性状全基因组关联分析 (MTAG):
- 方法逻辑: 由于峰值流速与平均梯度在遗传上高度相关(rg=0.99),研究者采用 MTAG 方法将上述定量表型与 AS 疾病 GWAS 进行联合分析,以利用不同性状间的遗传重叠来增强统计效能 (Figure 1c) 。
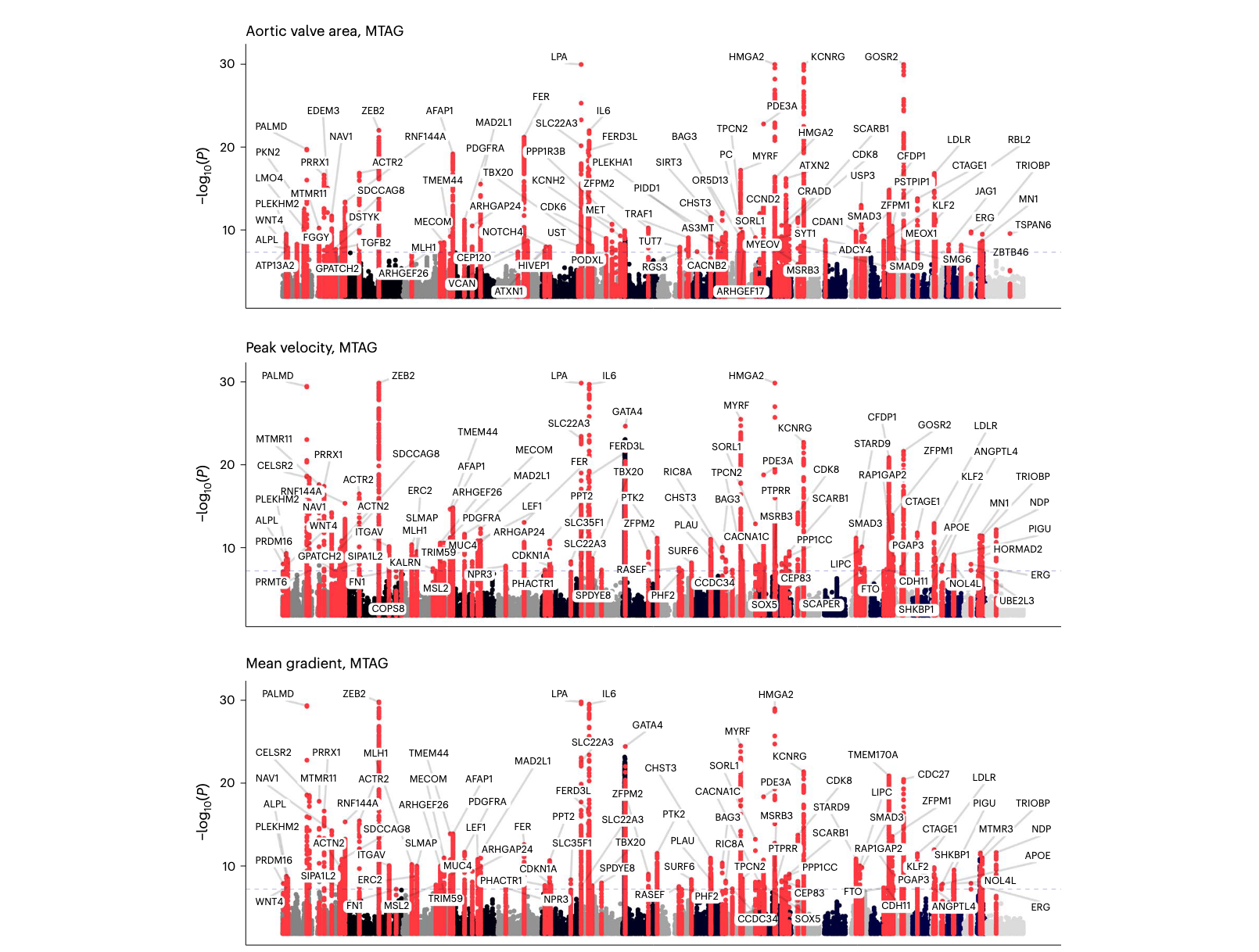
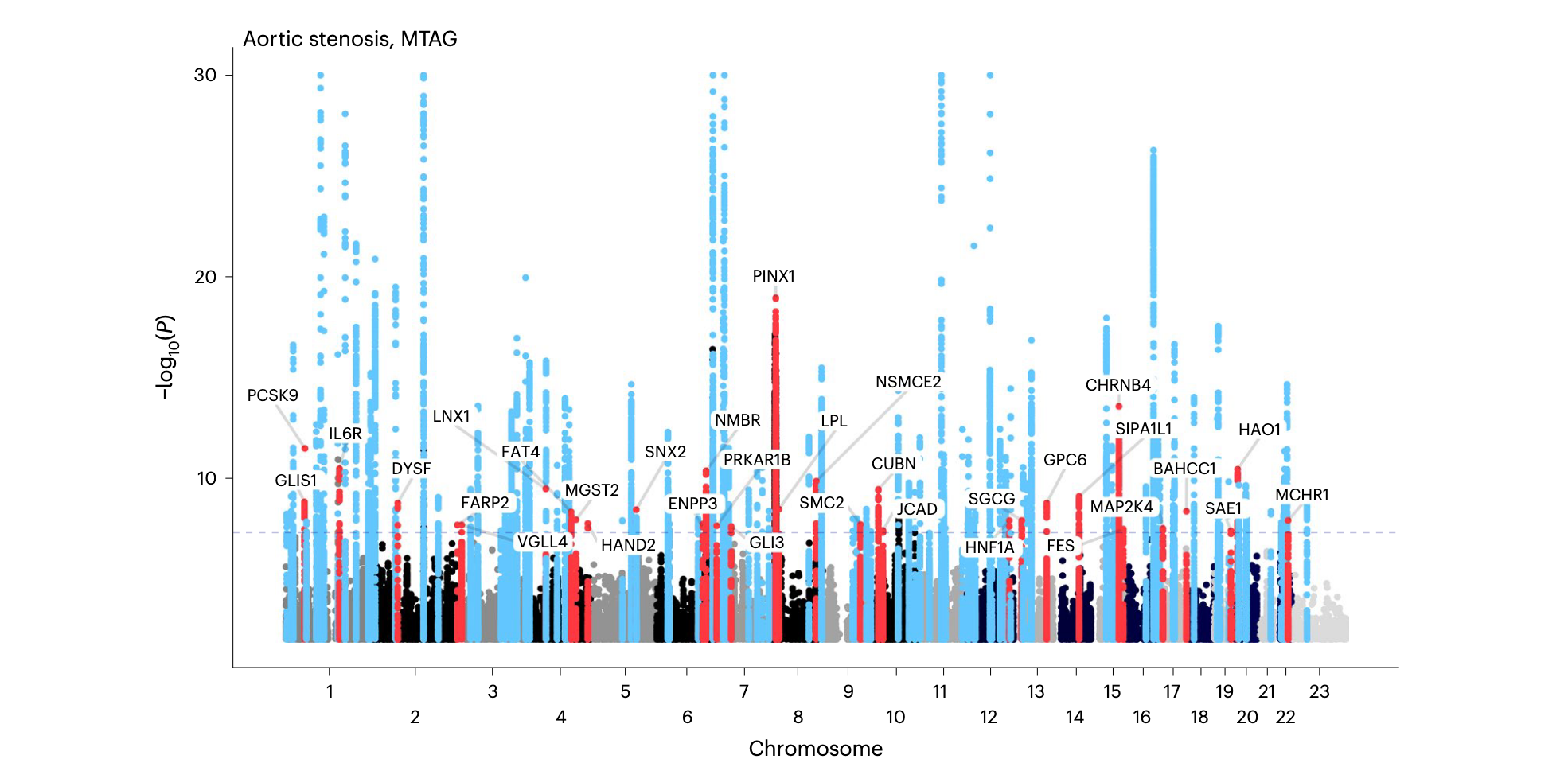
- 突破性结果: MTAG 分析使独立遗传位点的总数增加到 166个。其中 134 个位点与 AS 相关,比传统方法大幅增加了发现能力 (Figure 3) 。
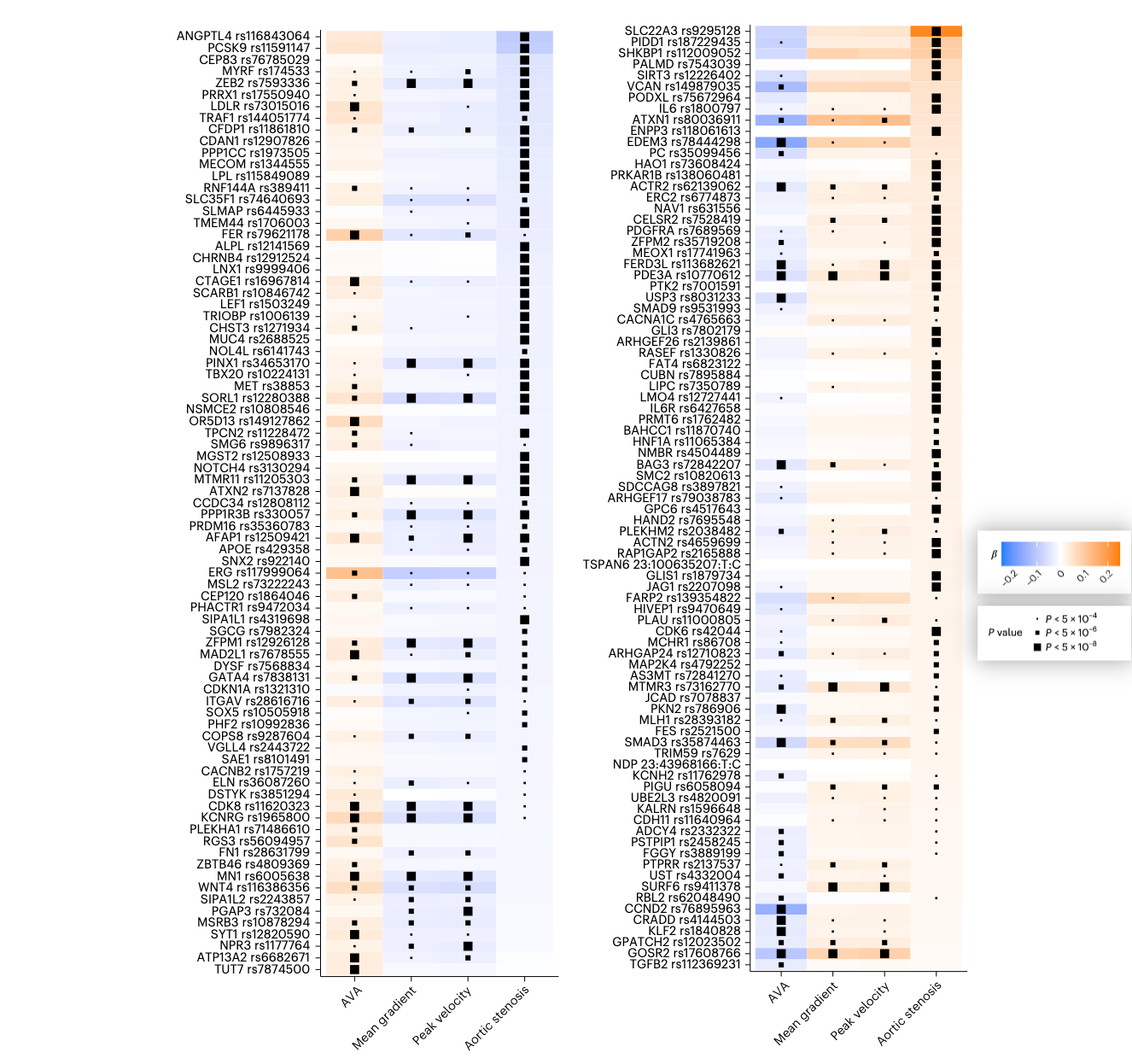
- 遗传一致性: 分析表明,正常人群中瓣膜功能指标的遗传波动与 AS 疾病风险高度一致。在 166 个位点中,有 102个 位点对功能指标和疾病风险均有显著贡献 (Figure 4) 。
生物学通路与细胞类型定位
通过 MAGMA 框架和单核转录组测序(scRNA-seq)数据,研究确定了变异发生作用的具体位置:
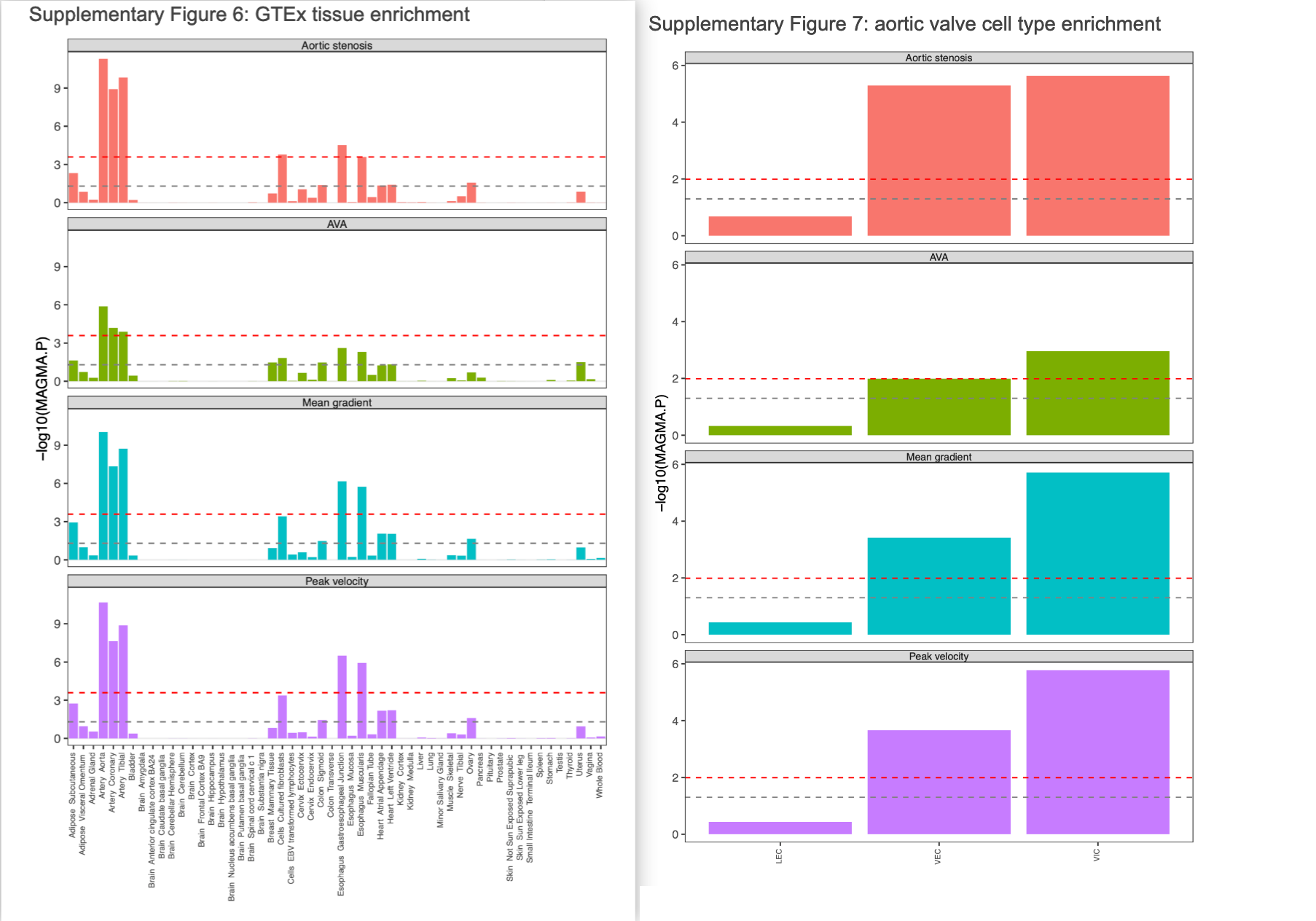
- 组织富集: 关联基因在主动脉、冠状动脉等动脉组织中表达最显著 (Supplementary Figure 6) 。
- 细胞图谱:
- 在主动脉瓣组织中,遗传信号主要集中在瓣膜间质细胞 (VIC) 和瓣膜内皮细胞 (VEC) (Supplementary Figure 7) 。
- 在左心室组织中,信号显著富集于“活化成纤维细胞”(Activated fibroblasts) (Supplementary Figure 9) 。
- 机制发现: 研究还识别出了与剪切应力响应(如 KLF2、PKN2)和炎症通路(如 IL6R、TRAF1)相关的基因位点,进一步阐明了 AS 发病的复杂性。
临床风险因素的因果推断 (MR)
作者利用遗传变异作为工具变量,验证了多个临床风险因素与瓣膜功能的因果关系 (Figure 1e) :
- 脂质指标: 研究证实 ApoB (低密度脂蛋白相关) 和 Lp(a) 对瓣膜面积减少和流速增加具有明确的因果破坏作用。这支持了早期针对所有含有 ApoB 的脂质进行降脂治疗可能预防 AS 的观点。 (Supplementary Table 17) 还说明了ApoA对AS没有因果作用。
- 血压与代谢: 收缩压 (SBP) 和 BMI 的增加与瓣膜功能减退存在因果关联。 (Supplementary Tables 18-19)
- 血磷的独特性: 血磷水平相关位点(如 FGF23)与 AS 疾病风险存在因果关系,但不显著。与之对比的是钙和维生素D在本研究中没有显示出对AS有因果作用。 (Supplementary Tables 18-19)
多基因风险评分 (PGS) 的临床预测价值
为了验证研究的临床应用潜力,研究者构建了包含约 110万个 变异位点的 MTAG PGS。
- 预测效能: 在 All of Us 队列(外部完全独立样本库)中,该评分表现优异:
- AS MTAG PGS 每增加一个标准差,新发 AS 的风险增加 1.64倍。
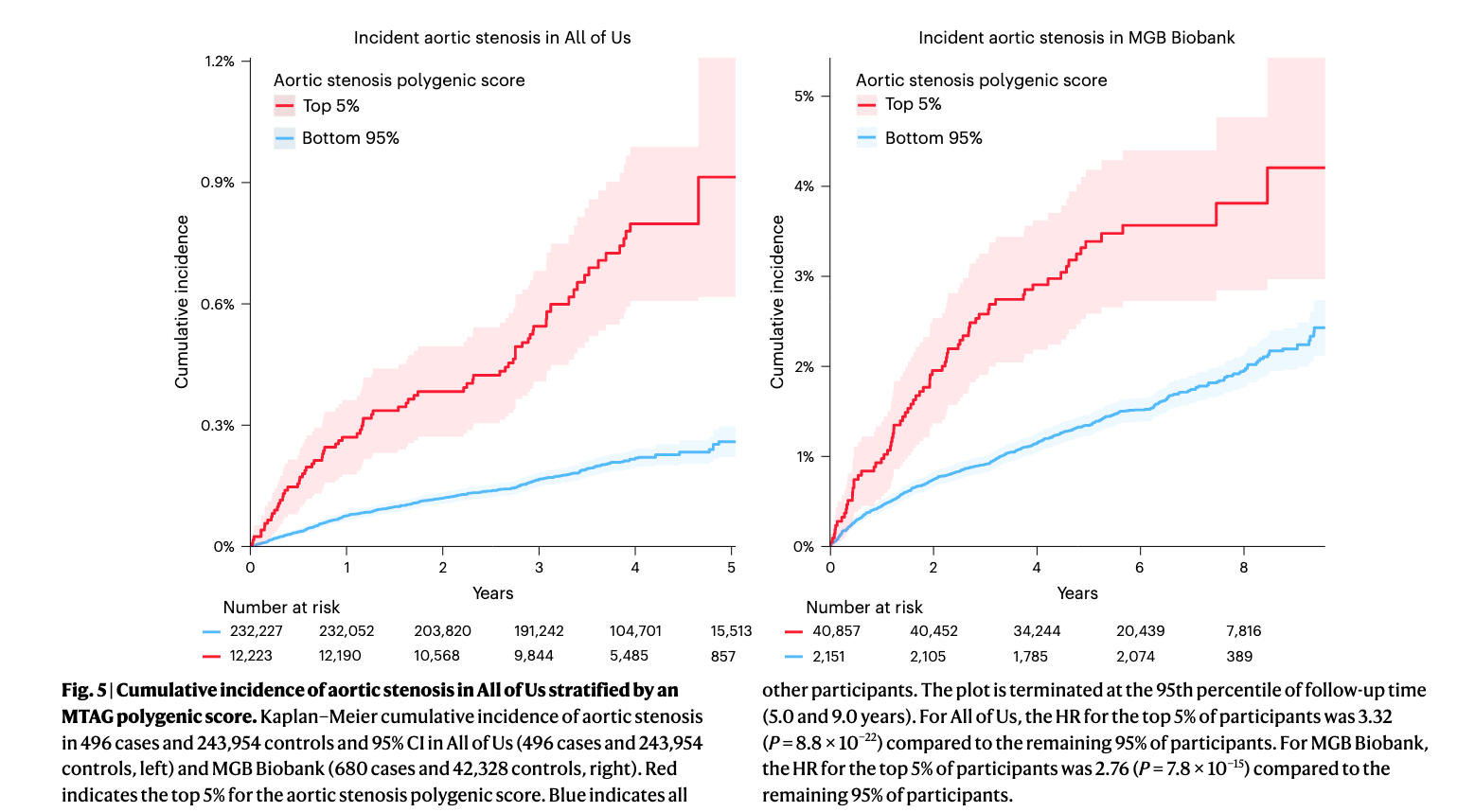
- 风险阶梯: 与普通人群相比,PGS 处于最高前 5% 的个体患病风险增加了 3.32倍 (Figure 5) 。
- 一致性: 在 Mass General Brigham (MGB) 生物样本库中,高风险(前 5%)个体的风险同样显著增加(2.76倍),证明了评分在不同医疗系统中的稳健性 (Figure 5) 。
讨论
遗传挖掘的范式演变:从“疾病诊断”到“定量内表型”
本研究最重要的贡献在于证明了定量内表型(Quantitative Endophenotypes)在遗传学研究中的巨大威力。传统的遗传学分析往往受限于临床诊断的“有或无”,而作者利用深度学习技术从约6万人的影像中提取出瓣膜流速、压力梯度等连续数值,捕捉到了健康人群中也存在的生理波动。这种方法将 AS 相关的遗传位点从以往研究的 32 个大幅扩展到了 166 个,证明了健康人群中瓣膜功能的正常变异与病理性狭窄在遗传上是高度一致的。这一发现打破了健康与疾病的绝对界限,暗示 AS 的风险实际上是由驱动瓣膜功能正常变异的相同遗传机制所决定的。
脂质与磷代谢:因果驱动因素的差异化角色
研究通过孟德尔随机化(MR)和多基因评分(PGS)深入探讨了代谢因素对瓣膜的损害。
- 脂质的早期破坏作用:
- 他汀类药物主要通过调节低密度脂蛋白(LDL)受体来降低血液中富含载脂蛋白 B(ApoB-rich)的脂质,其核心目标通常是低密度脂蛋白(LDL) 。
- 本研究结果证实了 ApoB(含载脂蛋白 B 的脂质) 和 Lp(a) 对瓣膜功能具有显著的因果破坏作用,且这些效应在健康人群中就已经开始显现。Lp(a) 也是一种含 ApoB 的脂质颗粒。然而,对于携带 LPA 基因变异的患者,即使在接受他汀类药物治疗的情况下,这类脂质仍会带来残余的心血管风险。
- 研究明确指出,LDLR(低密度脂蛋白受体基因)和 PCSK9 是调节血液中富含 ApoB 脂质水平的核心基因。这暗示了针对这些靶点的药物(如临床上常用的 PCSK9 抑制剂)是调节 ApoB 类脂质的重要手段。
- 磷代谢的后期进展作用: 相比之下,血磷水平(关联位点如 FGF23)展现出独特的致病模式:它显著增加临床 AS 的风险,但在健康人群中对正常的瓣膜流速几乎没有影响。这引导作者提出一个关键假设:磷代谢可能更多地参与瓣膜钙化的疾病进展阶段,而非初期的发病过程。
机械应力与炎症:瓣膜微环境的病理重塑
除了代谢因素,研究还识别出一系列反映瓣膜独特生理环境的遗传变异。
- 机械压力与血流感知: 瓣膜长期暴露于高剪切应力中,研究发现了与剪切力感知相关的基因,如 KLF2(保护瓣膜免于钙化的转录因子)和 PKN2(受机械受体激活调节血管张力),揭示了物理应力如何转化为生物病理信号。同时,遗传证据支持高收缩压(SBP)和高 BMI 是 AS 的直接因果风险因素,强调了血压控制在瓣膜保护中的核心地位。
- 炎症与细胞定位: 研究发现了 IL6R、TRAF1 等新的炎症相关位点,进一步巩固了炎症在 AS 中的作用。单核转录组分析将这些信号精确准确定位在成纤维细胞、**瓣膜间质细胞(VIC)和瓣膜内皮细胞(VEC)**中,为理解瓣膜纤维化和矿化提供了细胞层面的解析。
研究局限性
- 人群代表性: 研究样本主要源于 UK Biobank,存在“健康志愿者偏倚”,且参与者绝大多数为欧洲裔,结论在多元化人群中的普适性仍需验证。
- 验证需求: 尽管多性状分析(MTAG)在挖掘上很强大,但仍存在假阳性风险,在临床应用前(如干预血磷或胆固醇进行预防)仍需更多的功能性研究和临床试验验证。
临床转化展望:多基因评分驱动的精准预防
在应用层面,研究构建的 MTAG 多基因评分展示了强大的风险预测能力。在外部独立的 All of Us 队列验证中,处于遗传风险前 5% 的个体,其新发 AS 的风险比普通人群高出 3.32 倍。这为未来的临床实践提供了一个清晰的蓝图:通过 PGS 评分识别高危个体,并针对性地进行早期干预(如更早的血压管理和降脂治疗),从而在瓣膜发生不可逆损伤前阻断其病理进程。
对我们后续研究的启发
这种偏向于纯粹遗传学研究的逻辑和思路,在我们目前课题组的研究中很难进行模仿和复刻。但是本研究中所提供的一些特定的遗传位点、基因和通路等,是有深挖下去的意义的。例如研究中首次提到的 X 染色体上的 NDP 和 TSPAN6,或者是尚未被深入探索的 MN1。
而且这种顶级期刊通常会给我们启发一些病理机制的导向。比如本研究着重提到了机械应力感知: 研究发现了与剪切力感知相关的基因,如 KLF2 和 PKN2。这提示瓣膜病变不仅仅是生化过程,更是物理信号的转导。
本研究致力于探讨主动脉瓣功能及其与主动脉瓣狭窄(AS)风险相关的遗传变异。通过对UK Biobank中62902名参与者进行相差心血管磁共振成像(cMRI),结合深度学习技术,自动提取了三项关键的生理指标:峰值流速、平均压力梯度和主动脉瓣面积。研究利用多性状全基因组关联分析(MTAG),识别出与这些表型相关的遗传变异,从而提高新遗传位点的发现效率。此外,通过孟德尔随机化方法,探索了潜在的因果关系。结果显示,定量内表型的应用在遗传学研究中具有重要价值,有助于揭示主动脉瓣功能障碍与AS风险之间的遗传基础,为该疾病的预防和治疗提供新的视角与思路。



暂无评论内容